Die Carbonylverbindungen: Aldehyde und Ketone im Vergleich
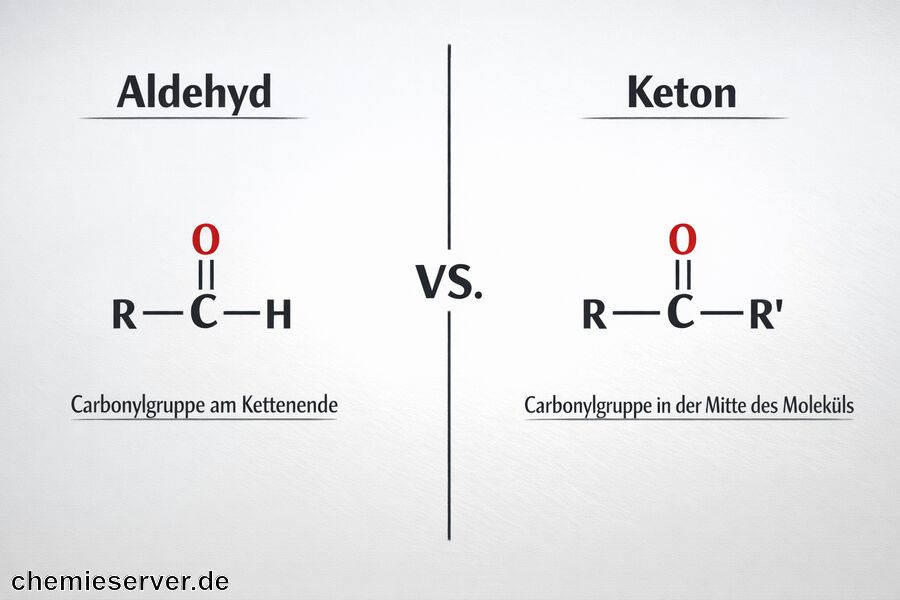
Die Wunder der organischen Chemie liegen in den vielfältigen Strukturen und Reaktionen, die Moleküle ermöglichen. Aldehyde und Ketone sind zwei wichtige Gruppen dieser Verbindungen, die oft für ähnliche Zwecke verwendet werden, sich jedoch in ihrer Struktur deutlich unterscheiden. Während Aldehyde die Carbonylgruppe terminal am Ende ihrer Kette tragen (R-CHO), befinden sich Ketone mit derselben Funktion innerhalb des Moleküls (R-CO-R‘). Diese Unterschiede beeinflussen nicht nur ihre chemische Reaktivität, sondern auch ihre typische Verwendung und Eigenschaften in verschiedenen Anwendungen.
Wichtiges am Anfang
- Aldehyde tragen die Carbonylgruppe terminal am Ende der Molekülkette.
- Ketone besitzen die Carbonylfunktion innerhalb der Struktur, z. B. an einem mittleren Kohlenstoff.
- Aldehyde haben mindestens ein Wasserstoffatom an der Carbonylgruppe.
- Ketone haben nur Alkylgruppen an die Carbonylgruppe gebunden, keine Wasserstoffatome.
- Beide reagieren in chemischen Reaktionen ähnlich, unterscheiden sich jedoch in Reaktivität und Stabilität.
Carbonylgruppe am Ende oder in der Mitte? Aldehyde tragen die Carbonylgruppe terminal am Ende
Ein zentrales Merkmal von Aldehyden ist die terminale Lage der Carbonylgruppe am Ende der Hauptkette. Diese Struktur erkennt man daran, dass die Carbonylfunktion als Endgruppe der Form R–CHO vorliegt, wobei das Carbonylkohlenstoffatom direkt mit einem Wasserstoffatom und einer Alkylgruppe verbunden ist. Aufgrund dieser Anordnung beginnt die Hauptkette nach der Carbonylgruppe, was sich auch klar in der Benennung der Verbindungen widerspiegelt. Dadurch lassen sich Aldehyde eindeutig von Ketonen unterscheiden, bei denen die Carbonylgruppe innerhalb der Kohlenstoffkette liegt.
Diese besondere Position der Carbonylgruppe beeinflusst maßgeblich die Reaktivität und die chemischen Eigenschaften von Aldehyden. In Strukturformeln oder Reaktionsschemata kann die terminale Carbonylgruppe leicht identifiziert werden. Zudem endet der Name von Aldehyden in der Regel auf -al, was die strukturelle Besonderheit sofort kenntlich macht. Dieses eindeutige Merkmal erleichtert die Zuordnung im Labor und die gezielte Verwendung von Aldehyden in chemischen Synthesen, da ihre Reaktionsmechanismen eng mit der Lage der funktionellen Gruppe verknüpft sind.
Ketone besitzen die Carbonylfunktion innerhalb der Struktur
Im Gegensatz zu Aldehyden, bei denen die Carbonylgruppe terminal am Ende der Molekülkette liegt, ist diese funktionelle Gruppe bei Ketonen innerhalb der Struktur angeordnet. Die Carbonylfunktion befindet sich an einem mittleren Kohlenstoffatom, das mit zwei Alkylresten verbunden ist (R–CO–R‘). Diese Anordnung prägt die chemischen Eigenschaften und die Reaktivität der Verbindung. In der Nomenklatur wird sie meist durch die Endung -on gekennzeichnet, die auf die zentrale Lage der Carbonylgruppe hinweist.
Ketone entstehen häufig durch die Oxidation sekundärer Alkohole oder durch Acylierungsreaktionen, bei denen die Carbonylgruppe innerhalb der Kohlenstoffkette erhalten bleibt. Da die funktionelle Gruppe nicht endständig ist, zeigen Ketone im Allgemeinen eine geringere Reaktivität als Aldehyde. Besonders gegenüber Oxidationsreaktionen sind sie deutlich stabiler, was ihnen in vielen chemischen Anwendungen Vorteile verschafft.
Die innenliegende Position der Carbonylgruppe beeinflusst auch die Wechselwirkung von Ketonen mit anderen Molekülen. Substituenten an den benachbarten Kohlenstoffatomen können die Reaktionsbereitschaft gezielt verändern. Dieser strukturelle Aufbau macht Ketone zu wichtigen Stoffklassen in der organischen Chemie, da sie vielseitig einsetzbar sind, etwa als Lösungsmittel oder als Zwischenprodukte in zahlreichen Synthesewegen und biologischen Prozessen.
„Die Chemie ist die große Königin der Wissenschaften, weil ihre Gesetze alle anderen Wissenschaften durchdringen.“ – Marie Curie
Aldehyde haben mindestens ein Wasserstoffatom an Bindung
Ein wesentliches Merkmal von Aldehyden ist das Vorhandensein von mindestens einem Wasserstoffatom an der Carbonylgruppe. Dieses Wasserstoffatom ist direkt an das Kohlenstoffatom der Carbonylfunktion gebunden und beeinflusst die chemischen Eigenschaften dieser Stoffklasse maßgeblich. Durch dieses gebundene Wasserstoffatom können Aldehyde besonders leicht an chemischen Reaktionen teilnehmen, vor allem an Oxidationsprozessen, bei denen sie zu Carbonsäuren weiterreagieren. Dadurch sind Aldehyde in der Regel reaktiver als Ketone, denen ein solches Wasserstoffatom an der Carbonylgruppe fehlt.
Strukturell trägt das Wasserstoffatom zur stärkeren Polarisierung der Carbonylgruppe bei. Dies erhöht die Reaktionsbereitschaft der Verbindung und begünstigt Additions- und Oxidationsreaktionen. In vielen Synthesen werden Aldehyde gezielt eingesetzt, da ihre Reaktionen oft unter vergleichsweise milden Bedingungen ablaufen und gut steuerbar sind.
Die Bindung mindestens eines Wasserstoffatoms an die Carbonylfunktion ist somit ein zentrales Unterscheidungsmerkmal von Aldehyden. Sie bestimmt sowohl den Aufbau als auch die Reaktivität dieser Verbindungen und wird in der Chemie gezielt genutzt, um Aldehyde selektiv umzuwandeln oder weiterzuverarbeiten.
Ketone haben nur Alkylgruppen an die Carbonylgruppe
Bei Ketonen ist das Kohlenstoffatom der Carbonylgruppe stets an zwei Alkylgruppen gebunden. Diese Alkylreste können unterschiedlich aufgebaut sein, häufig handelt es sich um Methyl- oder Ethylgruppen, die den strukturellen Rahmen des Ketonmoleküls bilden. Im Unterschied zu Aldehyden, bei denen am Carbonylkohlenstoff mindestens ein Wasserstoffatom gebunden ist, tragen Ketone ausschließlich Alkylgruppen an dieser Position. Dieser strukturelle Unterschied wirkt sich deutlich auf ihre chemischen Eigenschaften aus.
Die beiden Alkylgruppen schirmen die Carbonylfunktion teilweise ab und erhöhen dadurch die Stabilität der Verbindung. Ketone sind deshalb gegenüber Oxidationsreaktionen meist widerstandsfähiger als Aldehyde. Gleichzeitig beeinflussen die Alkylreste die Polarität, Löslichkeit und den Siedepunkt der Moleküle, was für ihre Verwendung in chemischen Prozessen eine wichtige Rolle spielt.
Insgesamt führt die ausschließliche Bindung von Alkylgruppen an der Carbonylgruppe dazu, dass Ketone häufig als stabile Lösungsmittel oder als Zwischenprodukte in organischen Synthesen eingesetzt werden. Ihre geringere Reaktivität im Vergleich zu Aldehyden macht sie gut kontrollierbar und vielseitig nutzbar in Industrie und Labor.
Chemisch reagieren beide ähnlich, unterscheiden sich in Struktur – Warum Aldehyde reaktiver sind als Ketone?
Aldehyde und Ketone besitzen beide die Carbonylgruppe, weshalb sie in vielen chemischen Reaktionen ein ähnliches Grundverhalten zeigen. So reagieren beide Stoffklassen häufig mit nukleophilen Teilchen und gehen typische Additionsreaktionen ein. Diese gemeinsame funktionelle Gruppe sorgt dafür, dass sich ihre grundlegenden Reaktionsmechanismen in vielen Fällen gleichen.
Trotz dieser Gemeinsamkeit zeigen sich deutliche Unterschiede in Reaktivität und Stabilität, die auf den strukturellen Aufbau zurückzuführen sind. Aldehyde lassen sich vergleichsweise leicht oxidieren, da am Carbonylkohlenstoff mindestens ein Wasserstoffatom gebunden ist. Dadurch können sie unter milden Bedingungen zu Carbonsäuren weiterreagieren. Ketone besitzen dagegen ausschließlich Alkylgruppen an der Carbonylfunktion und sind gegenüber Oxidationsmitteln deutlich widerstandsfähiger, sodass sie nur unter starken Bedingungen reagieren.
Insgesamt folgen Aldehyde und Ketone ähnlichen Reaktionsprinzipien, etwa bei Additions- oder Kondensationsreaktionen. Dennoch beeinflusst die unterschiedliche Lage und Substitution der Carbonylgruppe die Reaktionsgeschwindigkeit und das Reaktionsverhalten spürbar. Damit zeigt sich, dass beide Stoffklassen strukturell klar unterscheidbar sind, chemisch jedoch viele vergleichbare Reaktionswege besitzen.
Aldehyde oxidieren leicht – Ketone bleiben stabil
Typische Vertreter: Formaldehyd und Aceton
Ein typischer Vertreter der Aldehyde ist Formaldehyd (HCHO). Dabei handelt es sich um einen sehr reaktiven Stoff, der vor allem in der Konservierung und Desinfektion eingesetzt wird. Formaldehyd ist giftig und flüchtig, weshalb bei der Handhabung besondere Sicherheitsmaßnahmen erforderlich sind. Aufgrund seiner einfachen Struktur, bestehend aus einem Wasserstoffatom und einer Carbonylgruppe, lässt sich Formaldehyd leicht in chemische Reaktionen einbinden. Zudem spielt es eine wichtige Rolle bei der Herstellung von Kunststoffen, etwa von Harzen und Verbundwerkstoffen.
Im Gegensatz dazu ist Aceton (CH₃COCH₃) ein bekanntes Keton, das häufig als Lösungsmittel verwendet wird. Es besitzt zwei Methylgruppen, die an die Carbonylfunktion gebunden sind, was zu einer höheren chemischen Stabilität führt. Aceton ist in der Industrie weit verbreitet, zum Beispiel bei Reinigungsprozessen oder in der pharmazeutischen Produktion. Seine einfache Handhabung und guten Löslichkeitseigenschaften machen es zu einem Standardlösungsmittel in Laboren und industriellen Anwendungen. Während Formaldehyd aufgrund seiner hohen Reaktivität gezielt eingesetzt wird, überzeugt Aceton durch Stabilität und vielseitige Einsatzmöglichkeiten.
Unterschiede sichtbar in der Reaktionsfähigkeit und Verwendung
Die Unterschiede in der Reaktionsfähigkeit von Aldehyden und Ketonen sind klar erkennbar und wirken sich direkt auf ihre Verwendung in chemischen Prozessen aus. Aldehyde reagieren meist deutlich leichter mit Oxidationsmitteln, da an der Carbonylgruppe mindestens ein Wasserstoffatom gebunden ist. Dadurch lassen sie sich vergleichsweise einfach zu Carbonsäuren oxidieren oder als reaktive Zwischenstufen in Synthesen einsetzen. Diese Eigenschaft wird gezielt genutzt, um bestimmte Reaktionsabläufe effizient zu steuern.
Ketone hingegen zeichnen sich durch eine höhere chemische Stabilität aus. Da an ihrer Carbonylgruppe ausschließlich Alkylgruppen gebunden sind, sind sie gegenüber Oxidationsreaktionen wesentlich widerstandsfähiger. Diese Stabilität macht Ketone besonders geeignet für Anwendungen, bei denen Beständigkeit gefragt ist, etwa als Lösungsmittel oder als relativ inerte Reaktionspartner in der organischen Chemie.
Auch in der praktischen Nutzung spiegeln sich diese Unterschiede wider. Formaldehyd wird aufgrund seiner hohen Reaktivität in Konservierungs- und Desinfektionsmitteln eingesetzt, da er schnell mit biologischen Stoffen reagiert. Aceton dagegen dient vor allem als Lösungsmittel, bei dem gute Löslichkeit und chemische Stabilität im Vordergrund stehen. Insgesamt zeigt sich, dass Aldehyde vor allem durch ihre Reaktivität, Ketone hingegen durch ihre Stabilität charakterisiert sind, was ihre jeweiligen Einsatzgebiete bestimmt.
| Merkmal | Aldehyd | Keton | Beispiele & Verwendung |
|---|---|---|---|
| Position der Carbonylgruppe | Terminal, am Ende der Molekülstruktur | Innerhalb der Molekülstruktur (Mittelposition) | Formaldehyd (Desinfektionsmittel), Aceton (Lösungsmittel) |
| Anzahl der Wasserstoffatome an der Carbonylgruppe | Mindestens ein Wasserstoffatom | Keine Wasserstoffatome an der Carbonylgruppe | Aldehyde meist reaktiver, Ketone stabiler |
| Generelle Reaktionsfähigkeit | Reagiert häufig in Oxidations- und Reduktionsreaktionen | Weniger reaktiv, z. B. in Kondensationsreaktionen | Unterschiedliches chemisches Verhalten |
| Typische Vertreter | Formaldehyd, Benzaldehyd | Aceton, Cyclohexanon | Wichtig für organische Synthese und Industrie |