Was ist eine Disproportionierungsreaktion?
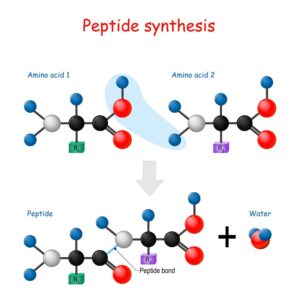
Die Disproportionierungsreaktion ist ein faszinierendes Phänomen in der Chemie, bei dem eine einzige Substanz gleichzeitig oxidiert und reduziert wird. Dies führt zur Bildung zweier verschiedener Produkte. Ein klassisches Beispiel dafür ist die Zersetzung von Wasserstoffperoxid, wobei ein Teil des Moleküls zu Sauerstoff oxidiert, während der andere Teil zu Wasser reduziert wird. Die Disproportionierungsreaktion wird auch als Selbstredoxreaktion bezeichnet.
Elektronentransfer spielt hierbei eine wesentliche Rolle, da es der Mechanismus ist, durch den die Reduktion und Oxidation erfolgen. Die beteiligten Reaktanten zeigen unterschiedliche Oxidationszahlen, was sowohl die Funktion als auch das Verständnis dieser Reaktion verdeutlicht.
Disproportionierungen sind nicht nur auf klassische chemische Reaktionen beschränkt; sie finden ebenso in biologischen Systemen statt. Zum Beispiel ist die katalytische Aktivität bestimmter Enzyme auf solche Reaktionen zurückzuführen.
Bei industriellen Anwendungen werden häufig Katalysatoren eingesetzt, um diese Reaktionen zu beschleunigen und effizienter zu gestalten. Vor allem Edelmetalle wie Platin oder Palladium spielen hier eine Schlüsselrolle.
Umweltaspekte sind ebenfalls relevant, da einige Disproportionierungsreaktionen umweltfreundliche Alternativen zu herkömmlichen Verfahren bieten können. Das Verständnis der thermodynamischen und kinetischen Aspekte solcher Reaktionen hilft dabei, Prozesse nachhaltiger zu gestalten und zu optimieren.
Das Wichtigste in Kürze
- Disproportionierungsreaktionen umfassen gleichzeitige Oxidation und Reduktion eines Elements zu zwei verschiedenen Produkten.
- Ein Beispiel ist die Zersetzung von Wasserstoffperoxid zu Wasser und Sauerstoff.
- Katalysatoren wie Platin beschleunigen und optimieren diese Reaktionen.
- Sind thermodynamisch und kinetisch bestimmt, oft in der Elektrochemie wichtig.
- Spielen in biologischen und industriellen Prozessen, wie Enzymen und Wasserstoffperoxid-Herstellung, eine große Rolle.
Eine Disproportionierungsreaktion ist eine chemische Reaktion, bei der ein Stoff sowohl oxidiert als auch reduziert wird. Dabei wird der gleiche Stoff gleichzeitig zu einem stärker und einem schwächer oxidierten Produkt umgewandelt. Dies bedeutet, dass ein Teil des Stoffes oxidier wird, während ein anderer Teil desselben Stoffes reduziert wird.
Beispiele
- Disproportionierungsreaktion von Wasserstoffperoxid (H2O2) zu Wasser (H2O) und Sauerstoff (O2): 2H2O2 -> 2H2O + O2
- Disproportionierungsreaktion von Chlor (Cl2) zu Chloridionen (Cl-) und Hypochlorit-Ionen (ClO-): 2Cl2 -> 2Cl- + ClO-
- Disproportionierungsreaktion von Stickstoffdioxid (NO2) zu Salpetersäure (HNO3) und Stickstoffmonoxid (NO): 3NO2 + H2O -> 2HNO3 + NO
- Disproportionierungsreaktion von Ozon (O3) zu Sauerstoff (O2) und Ozonid-Ionen (O3-): 2O3 -> 3O2 + O3-
- Disproportionierungsreaktion von Bromwasserstoff (HBr) zu Bromidionen (Br-) und Brom (Br2): 3HBr -> 2Br- + Br2
- Disproportionierungsreaktion von Schwefeldioxid (SO2) zu Schwefelsäure (H2SO4) und Schwefel (S): 2SO2 + O2 -> 2H2SO4 + S
- Disproportionierungsreaktion von Dichromat-Ionen (Cr2O7^2-) zu Chrom(III)-Ionen (Cr^3+) und Chromat-Ionen (CrO4^2-): 14H^+ + Cr2O7^2- + 6e^- -> 2Cr^3+ + 7H2O
- Disproportionierungsreaktion von Wasserstoffbromid (HBr) zu Bromidionen (Br-) und elementarem Brom (Br2): 4HBr -> 3Br- + Br2
- Disproportionierungsreaktion von Iodat-Ionen (IO3-) zu Iodidionen (I-) und elementarem Iod (I2): 5IO3- + 6I- + 6H^+ -> 3I2 + 3H2O
Definition der Disproportionierungsreaktion
Eine Disproportionierungsreaktion ist eine spezielle Art von Redox-Reaktion, bei der ein einzelnes chemisches Element gleichzeitig oxidiert und reduziert wird. Dies bedeutet, dass das gleiche Element in einem Molekül oder einer Verbindung zwei unterschiedliche Oxidationsstufen annimmt.
Während einer solchen Reaktion findet ein Elektronentransfer innerhalb des Systems statt. Konkret geht eines der Atome des Ausgangsstoffes Elektronen ab, wodurch es oxidiert wird, während ein anderes Atom derselben Substanz diese Elektronen aufnimmt und somit reduziert wird. Hier kommen die Konzepte der Reduktion und Oxidation ins Spiel, da eine Erhöhung bzw. Erniedrigung der Oxidationszahlen des zentralen Elements erfolgt.
Ein Beispiel für eine solche Reaktion ist die Zersetzung von Wasserstoffperoxid (H2O2) in Wasser (H2O) und Sauerstoff (O2). In dieser Reaktion fungiert das Wasserstoffperoxid sowohl als Oxidationsmittel als auch als Reduktionsmittel, was zur Bildung unterschiedlicher Produkte führt.
Disproportionierungsreaktionen sind von großer Bedeutung in der Elektrochemie und insbesondere in galvanischen Zellen und Batterien. Sie spielen auch eine entscheidende Rolle bei der Herstellung von Edelmetallen und der Berechnung der Spannungsreihe.
Chemie ist die Brücke zwischen Physik und Biologie. Sie zeigt uns, wie Elektronentransfer und Redoxreaktionen das Leben und unsere Technologien ermöglichen. – Wilhelm Ostwald
| Begriff | Beschreibung |
|---|---|
| Elektronentransfer | Der Prozess, bei dem Elektronen von einem Atom oder Molekül auf ein anderes übertragen werden, was zu Reduktion und Oxidation führt. |
| Oxidationszahlen | Eine willkürlich zugewiesene Zahl, die die Anzahl der Elektronen angibt, die ein Atom in einer Redox-Reaktion abgibt oder aufnimmt. |
| Oxidationsmittel | Ein Stoff, der Elektronen aufnimmt und dadurch oxidiert wird, indem er selbst reduziert wird. |
| Reduktionsmittel | Ein Stoff, der Elektronen abgibt und dadurch reduziert wird, indem er selbst oxidiert wird. |
| Reduktion | Der Gewinn von Elektronen durch ein Atom, Ion oder Molekül. |
| Oxidation | Der Verlust von Elektronen durch ein Atom, Ion oder Molekül. |
| Edelmetalle | Metalle wie Platin und Palladium, die in der Regel nicht korrodieren und oft als Katalysatoren genutzt werden. |
| Spannungsreihe | Eine Auflistung von Halbzellenpotenzialen, die die Fähigkeit eines Elements zeigt, als Oxidations- oder Reduktionsmittel zu fungieren. |
| Galvanische Zelle | Ein elektrochemischer Apparat, in dem chemische Energie in elektrische Energie umgewandelt wird. |
| Elektrochemie | Das Studium der chemischen Prozesse, die Elektronenbewegungen in Lösungen oder durch elektrische Leiter beinhalten. |
Beispiele aus Chemie und Biologie
Ein klassisches Beispiel einer Disproportionierungsreaktion in der Chemie ist die Reaktion von Chlor in Wasser. Hierbei disproportioniert Chlor (Cl₂) zu Salzsäure (HCl) und Hypochloriger Säure (HClO). Diese Reaktion kann durch folgende Gleichung dargestellt werden:
Cl₂ + H₂O → HCl + HClO
Chlor hat dabei eine Oxidationszahl von 0 im Cl₂-Molekül, welche in der HCl-Komponente auf -1 reduziert und in der HClO-Komponente auf +1 oxidiert wird. Dies zeigt anschaulich den gleichzeitigen Elektronentransfer zwischen Reduktion und Oxidation.
Auch in der Biologie sind Disproportionierungsreaktionen wichtig. Ein bekanntes Beispiel ist die Verarbeitung des Superoxid-Radikals (O₂⁻), welches in Zellen entsteht. Mittels spezieller Enzyme wie der Superoxiddismutase wird Superoxid disproportioniert:
2 O₂⁻ + 2 H⁺ → O₂ + H₂O₂
Hierbei handelt es sich um eine Redoxreaktion, bei der ein Teil des Superoxid-Ions zu Sauerstoff oxidiert (Oxidationszahl von -1 auf 0) und ein Teil zu Wasserstoffperoxid reduziert wird (Oxidationszahl von -1 auf -2).
Diese Beispiele verdeutlichen, wie vielseitig und wichtig Disproportionierungsreaktionen sowohl in der chemischen als auch biologischen Welt sind. Sie spielen eine bedeutende Rolle bei verschiedenen biochemischen Prozessen und industriellen Anwendungen, da sie oft zur effizienten Umwandlung und Nutzung von chemischen Stoffen beitragen.
Mechanismen und beteiligte Reaktanten
Mechanismen und beteiligte Reaktanten
Die Disproportionierungsreaktion ist eine spezielle Art der Redoxreaktionen, bei denen ein einzelner Stoff gleichzeitig als Oxidationsmittel und Reduktionsmittel agiert. Dadurch werden Elektronen sowohl aufgenommen als auch abgegeben, was zu einer Aufspaltung des Ausgangsmaterials in zwei verschiedene Produkte führt.
Ein klassisches Beispiel ist die Zersetzung von Wasserstoffperoxid (H₂O₂). Dabei zerfällt das H₂O₂ in Wasser (H₂O) und Sauerstoff (O₂), wobei Wasserstoffperoxid gleichzeitig oxidiert und reduziert wird:
\[ 2 H_2O_2 \rightarrow 2 H_2O + O_2 \]
Dies verdeutlicht, wie ein einzelnes Molekül in unterschiedliche Oxidationszustände überführt werden kann. Die beteiligten Reaktanten sind hier Wasserstoffperoxid, welches sowohl als Reduktionsmittel fungiert, indem es Sauerstoff freisetzt, als auch als Oxidationsmittel, indem es Wasser bildet.
Eine weitere bekannte Disproportionierung ist die Reaktion von Chlor in alkalischer Lösung:
\[ 3 Cl_2 + 6 OH^- \rightarrow 5 Cl^- + ClO_3^- + 3 H_2O \]
Chlor (Cl₂) disproportioniert dabei in Chlorid (Cl⁻) und Chlorat (ClO₃⁻).
Diese Reaktionen spielen eine bedeutende Rolle in vielen Bereichen der Elektrochemie und chemischen Industrie. Sie erfordern häufig präzise Bedingungen, um gezielt abzulaufen, da die Stabilität der resultierenden Verbindungen stark von den Oxidationszahlen der Elemente abhängt sowie dem Vorhandensein geeigneter Katalysatoren und spezifischer Temperatur- und Druckbedingungen.
Vor- und Nachteile der Reaktion
Ein bedeutender Vorteil der Disproportionierungsreaktion ist, dass sie die Möglichkeit bietet, ein Element simultan zu oxidieren und zu reduzieren. Dies führt zur Bildung von zwei verschiedenen chemischen Spezies aus einem einzigen Ausgangsstoff.
Dieser Prozess kann in bestimmten Industriezweigen wirtschaftlich vorteilhaft sein, vor allem, wenn edle Metalle wie Gold oder Platin beteiligt sind. Ein bemerkenswertes Beispiel ist die Anwendung bei der Gewinnung reiner Edelmetalle aus Erzen.
Nachteilig hingegen ist, dass solche Reaktionen oft eine genaue Kontrolle der Reaktionsbedingungen benötigen. Temperatur, Druck und die Konzentration der Reaktanten müssen genau überwacht werden, um das gewünschte Resultat zu erzielen. Dies kann die Prozesskosten erheblich steigern.
Ein weiterer Nachteil liegt in den thermodynamischen Beschränkungen einiger Disproportionierungsreaktionen. Nicht alle Reaktionen verlaufen spontan, was bedeutet, dass zusätzliche Energie erforderlich sein könnte. Außerdem können unerwünschte Nebenprodukte entstehen, die sorgfältig getrennt und entsorgt werden müssen.
In Bezug auf die Kinetik unterliegt die Geschwindigkeit vieler solcher Reaktionen der Anwesenheit von Katalysatoren, die den Elektronentransfer erleichtern. Daher hängt der Erfolg einer Disproportionierungsreaktion stark von der Wahl des richtigen Katalysators ab, was weitere Forschung und Entwicklung erfordert.
Zusammengefasst bieten Disproportionierungsreaktionen faszinierende Möglichkeiten, stellen jedoch auch Herausforderungen dar, die es sorgfältig zu bewältigen gilt.
Industrielle Anwendungen und Verfahren
Industrielle Anwendungen der Disproportionierungsreaktion finden sich in vielen Bereichen, darunter die chemische Industrie und die Metallurgie. Ein klassisches Beispiel ist die Synthese von Chlor aus Chlorwasserstoff durch die Oxidation an einem Anodenraum und gleichzeitiger Reduktion an einem Kathodenraum in einer Elektrolysezelle.
In diesem Prozess spielen Reduktion und Oxidation zentrale Rollen, bei denen Chlor sowohl als Oxidationsmittel als auch als Reduktionsmittel fungieren kann. Daher ist das Verständnis der beteiligten Oxidationszahlen entscheidend für die Steuerung der Reaktion.
Die Herstellung von Wasserstoffperoxid ist ein weiteres bedeutendes industrielles Beispiel. Hierbei wird Anthrachinon in einem zweistufigen Prozess zunächst reduziert, um Hydroanthrachinon zu bilden, welches anschließend relauntert oxidiert wird, um Wasserstoffperoxid zu erzeugen.
Auch in der Elektrochemie hat diese Reaktionskomponente Anwendung gefunden, insbesondere zur Gewinnung von Edelmetallen wie Gold und Silber aus Erzen durch elektrolytische Verfahren. Die Spannungsreihe hilft dabei, die Reihenfolge der reduzierbaren Ionen festzulegen, was wiederum zu effizienteren Prozessen führt.
Galvanische Zellen nutzen ebenfalls Prinzipien der Disproportionierung, indem sie zwischen den verschiedenen Redoxpaaren elektrische Energie umwandeln und speichern. Wichtig ist hierbei die Kontrolle über den Elektronentransfer, um stabile und langanhaltende Batterien zu gewährleisten.
Solche krozialen Anwendungen unterstreichen die Bedeutung der Thermodynamik und Kinetik dieser Reaktionen. Umweltaspekte spielen hier eine wichtige Rolle, da die Minimierung von Abfallprodukten und Optimierung der Ausbeute wesentliche Ziele sind.
| Begriff | Bedeutung | Beispiele |
|---|---|---|
| Disproportionierung | Eine Redoxreaktion, bei der ein Element gleichzeitig oxidiert und reduziert wird | 2 H₂O₂ → 2 H₂O + O₂ |
| Redoxreaktion | Eine chemische Reaktion, bei der Elektronen zwischen Atomen ausgetauscht werden | Z.B. Reaktionen in Batterien |
| Superoxiddismutase | Ein Enzym, das Superoxid-Radikale disproportioniert | 2 O₂⁻ + 2 H⁺ → O₂ + H₂O₂ |
Thermodynamische und kinetische Aspekte
Bei der Betrachtung der thermodynamischen und kinetischen Aspekte einer Disproportionierungsreaktion ist es wichtig, zwischen diesen beiden Konzepten zu unterscheiden. Die Thermodynamik bezieht sich auf die Energetik der Reaktion, also darauf, ob eine Reaktion spontan abläuft oder nicht. Spontan bedeutet hierbei, dass die Reaktion ohne äußere Einwirkung stattfindet.
Ein zentrales Konzept dabei ist das Gibbs’sche freie Energie ∆G. Wenn ∆G negativ ist, läuft die Reaktion spontan ab. Beispielsweise hängt die Chrom-Disproportionierung stark von den Oxidationszahlen und der Elektronenkonfiguration ab.
Die Kinetik dagegen beschäftigt sich mit der Geschwindigkeit, mit der eine Reaktion abläuft. Dies wird durch verschiedene Faktoren wie Temperatur, Konzentration der Reaktanten und das Vorhandensein eines Katalysators beeinflusst. Katalysatoren spielen eine erhebliche Rolle dabei, sowohl die Geschwindigkeit als auch die Selektivität der Reaktion zu erhöhen oder spezifische Pfade zu bevorzugen.
In vielen Fällen gilt: Selbst wenn eine Disproportionierungsreaktion thermodynamisch begünstigt ist, könnte sie aufgrund kinetischer Hindernisse sehr langsam verlaufen. Daher sind nicht nur die Energiediagramme, sondern auch Aktivierungsenergien relevant. Diese beschreiben die benötigte Energie, um die Reaktion in Gang zu setzen.
Besonders im industriellen Kontext möchte man diese Effekte optimieren. Zum Beispiel können Edelmetalle als Katalysatoren verwendet werden, um die Reaktionskinetik zu verbessern, was wiederum Einfluss auf die Wirtschaftlichkeit der Verfahren hat.
Zusammengefasst bestimmen sowohl thermodynamische als auch kinetische Aspekte das Verhalten und die Realisierbarkeit von Disproportionierungsreaktionen in praktischen Anwendungen.
Katalysatoren, die Reaktionen beeinflussen
Ein wesentlicher Aspekt der Disproportionierungsreaktion sind Katalysatoren, die diese Reaktionen sowohl in ihrer Geschwindigkeit als auch in ihrer Ausbeute beeinflussen können. Katalysatoren sind Substanzen, die die Aktivierungsenergie einer chemischen Reaktion senken und dabei selbst unverändert bleiben. In vielen Fällen führen sie zu einem schnellerem Erreichen des Gleichgewichts.
Ein Beispiel hierfür sind Übergangsmetalle wie Palladium oder Platin, die häufig bei Disproportionierungsreaktionen eingesetzt werden, um die Selektivität und Effizienz der Reaktion zu verbessern. Diese Metalle fördern den Elektronentransfer zwischen verschiedenen Oxidationsstufen der Reaktanten und sorgen somit für eine kontrollierte Abfolge der Reduktion und Oxidation.
Auch Enzyme in biologischen Systemen wirken ähnlich wie katalytische Metalle, indem sie biochemische Disproportionierungen beschleunigen. Hierbei spielen einige Proteine eine Schlüsselrolle, indem sie spezifische Reaktionswege ermöglichen und so bestimmte Stoffwechselprozesse regulieren.
Die Verwendung von Katalysatoren bietet zahlreiche Vorteile, darunter niedrigere Betriebstemperaturen und -drücke sowie eine verringerte Nebenproduktbildung. Dies trägt nicht nur zur Wirtschaftlichkeit sondern auch zur Umweltfreundlichkeit industrieller Prozesse bei. Obgleich die Anschaffungskosten für Edelmetallkatalysatoren hoch sein können, amortisieren sich diese durch die verlängerte Lebensdauer und erhöhte Prozessausbeute.
Insgesamt tragen Katalysatoren entscheidend dazu bei, Disproportionierungsreaktionen effizient und nachhaltig durchzuführen, indem sie essenzielle Mechanismen im Elektronentransfer verbessern.
Unterschied zwischen Disproportionierungsreaktion und Redoxredaktion
Eine Disproportionierungsreaktion ist tatsächlich eine spezielle Art von Redoxreaktion, bei der derselbe Stoff sowohl oxidiert als auch reduziert wird. Daher ist eine Disproportionierungsreaktion eine Form der Redoxreaktion. Es gibt Unterschiede zwischen einer Disproportionierungsreaktion und einer normalen Redoxreaktion. In einer Disproportionierungsreaktion reagiert derselbe Stoff sowohl als Reduktionsmittel als auch als Oxidationsmittel, was zu unterschiedlichen Oxidationsstufen desselben Elements führt. Bei einer normalen Redoxreaktion hingegen findet ein Elektronentransfer zwischen zwei verschiedenen Stoffen statt, bei dem einer oxidiert wird und der andere reduziert wird.
Ein Beispiel für eine Disproportionierungsreaktion ist die Reaktion von Chlor in Wasser, bei der Chlor zu Chloridionen (reduziert) und Chlorat(I)-Ionen (oxidier) reagiert:
Diese Reaktion von Chlor in Wasser ist ein Beispiel für eine Disproportionierungsreaktion, da Chlor sowohl zu Chloridionen (reduziert) als auch zu Chlorat(I)-Ionen (oxidiert) reagiert.
Disproportionierungsreaktion von Chlor in Wasser: 3Cl2 + 6H2O -> 5Cl- + ClO- + 6H+
Ein Beispiel für eine Redoxreaktion ist die Reaktion von Eisen mit Kupfersulfat, wobei Eisen zu Eisen(II)-Ionen oxidiert wird und Kupfer(II)-Ionen zu elementarem Kupfer reduziert werden:
Diese zweite Reaktion von Eisen mit Kupfersulfat ist ein Beispiel für eine Redoxreaktion, da Eisen zu Eisen(II)-Ionen oxidiert wird und Kupfer(II)-Ionen zu elementarem Kupfer reduziert werden.
Redoxreaktion von Eisen mit Kupfersulfat: Fe + CuSO4 -> FeSO4 + Cu
Umweltaspekte und Nachhaltigkeit berücksichtigen
Die nachhaltige Gestaltung von Disproportionierungsreaktionen hat eine wachsende Bedeutung vor dem Hintergrund der ökologischen Verantwortung.
Verantwortungsvolle Chemie
Ein wichtiger Aspekt ist die Minimierung von Abfällen und Emissionen. Durch den optimierten Einsatz von Reaktanten und Katalysatoren kann die Umweltbelastung reduziert werden. Der Einsatz von umweltfreundlichen Katalysatoren, wie beispielsweise bestimmte Edelmetalle, spielt dabei eine zentrale Rolle.
Rohstoffeffizienz
Effiziente Rückgewinnungsmethoden für eingesetzte Materialien sind ebenfalls bedeutend. In Prozessen, in denen Edelmetalle als Katalysatoren verwendet werden, sollten Recyclingmethoden implementiert werden, um den Materialverbrauch zu reduzieren und Ressourcen zu schonen.
Erneuerbare Energien
Die Anwendung von Elektrochemie zur Initiierung von Disproportionierungsreaktionen bietet zusätzliche Nachhaltigkeitsvorteile. Hierbei können erneuerbare Energiequellen genutzt werden, um elektrische Energie bereitzustellen. Beispielsweise könnte die Energie aus einer Galvanischen Zelle kommen, die durch Photovoltaik oder Windenergie gespeist wird.
Durch diese Ansätze lassen sich nicht nur ökologische Vorteile erzielen, sondern langfristig auch wirtschaftliche Einsparungen aufgrund effizienterer Prozesse und geringerer Materialkosten.