Anorganische Stoffe: Definition und Bedeutung
Anorganische Stoffe umfassen eine Vielzahl von chemischen Verbindungen, die vor allem durch das Fehlen von Kohlenstoff charakterisiert sind. Typische anorganische Substanzen beinhalten Metalle, Minerale, Salze, Säuren und Basen. Während organische Chemie sich primär um Kohlenstoffverbindungen dreht, beschäftigt sich die anorganische Chemie mit einer breiten Palette von Materialien.
Beispiele für anorganische Stoffe sind unter anderem Oxide, Halogene, Ionenverbindungen sowie Edelgase. Diese Stoffe spielen eine essenzielle Rolle in verschiedenen Bereichen des täglichen Lebens sowie in der Industrie. Von Anorganische Pigmente für Farben bis hin zu Erze für die Metallproduktion, die Anwendungen und Ausprägungen dieser Verbindungen sind vielfältig und weitreichend.
Interessanterweise zeigen viele anorganische Stoffe beeindruckende physikalische und chemische Eigenschaften. Dies ermöglicht ihre Verwendung in technologischen Innovationen wie Katalysatoren und Halbleitern. Auch im Bauwesen und der Medizin finden spezifische anorganische Materialien zahlreiche Anwendungen, was ihren hohen Stellenwert noch einmal verdeutlicht.
Das Wichtigste in Kürze
- Anorganische Stoffe umfassen Metalle, Oxide, Salze, Säuren und Basen ohne Kohlenstoff-Wasserstoff-Bindungen.
- Metalle sind leitfähig, duktil und stark; Nichtmetalle sind unterschiedlich, oft schlecht leitend und weniger dicht.
- Wichtige Anwendungen im Bauwesen (z.B. Beton, Stahl) und der Medizin (z.B. Calciumphosphate, Silbernitrat).
- Anorganische Stoffe sind entscheidend in Katalysatoren (z.B. Eisen, Platin) und Halbleitern (z.B. Silizium, Galliumarsenid).
- Umweltfreundliche anorganische Materialien fördern nachhaltige Technologien und reduzieren Umweltbelastungen (z.B. recyclingfähiges Aluminium).
Anorganische Stoffe sind chemische Verbindungen und Elemente, die in der Regel keinen Kohlenstoff enthalten. Die Abgrenzung zur organischen Chemie erfolgt hauptsächlich über das Fehlen von Kohlenstoff-Wasserstoff-Bindungen (Kohlenwasserstoffe).
Definition und Abgrenzung der anorganischen Stoffe
Anorganische Stoffe werden traditionell definiert als:
- Alle chemischen Elemente außer Kohlenstoff.
- Alle Verbindungen, die keinen Kohlenstoff enthalten.
- Einige Ausnahmen von kohlenstoffhaltigen Verbindungen, die ähnliche Eigenschaften wie typische anorganische Stoffe aufweisen.
Die Abgrenzung zur organischen Chemie erfolgt hauptsächlich über das Fehlen von Kohlenstoff-Wasserstoff-Bindungen (Kohlenwasserstoffe).
Beispiele für anorganische Stoffe
Wichtige Beispiele anorganischer Stoffe
- Elemente:
- Metalle: Gold, Silber, Kupfer
- Nichtmetalle: Schwefel, Sauerstoff, Stickstoff
- Salze:
- Natriumchlorid (Kochsalz)
- Calciumcarbonat (Kalk)
- Oxide:
- Kohlenstoffdioxid (CO₂)
- Kohlenstoffmonoxid (CO)
- Säuren und Basen:
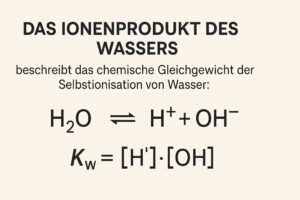
- Wasser (H₂O):
- Eine der wichtigsten anorganischen Verbindungen.
Ausnahmen mit Kohlenstoff
Einige kohlenstoffhaltige Verbindungen werden dennoch zur anorganischen Chemie gezählt:
- Kohlenstoffoxide (CO, CO₂)
- Carbonate
- Cyanide, Cyanate, Thiocyanate
- Carbide
| Stoff | Erklärung |
|---|---|
| Wasser (H2O) | Wasser ist eine anorganische Verbindung aus Wasserstoff und Sauerstoff. Es ist eine der wichtigsten Verbindungen für das Leben auf der Erde und spielt eine entscheidende Rolle in chemischen Reaktionen. |
| Kochsalz (NaCl) | Kochsalz ist ein anorganisches Salz, das aus Natrium- und Chloridionen besteht. Es wird als Gewürz und Konservierungsmittel verwendet und ist in der Natur weit verbreitet, z.B. in Meerwasser und in Salzminen. |
| Kohlendioxid (CO2) | Kohlendioxid ist eine Verbindung aus Kohlenstoff und Sauerstoff, die in der Atmosphäre vorkommt und für den Treibhauseffekt verantwortlich ist. Es wird auch bei der Herstellung von kohlensäurehaltigen Getränken verwendet. |
| Calciumoxid (CaO) | Calciumoxid ist eine anorganische Verbindung, die als Branntkalk bekannt ist. Es wird in der Industrie zur Herstellung von Zement und in der Landwirtschaft als Düngemittel eingesetzt. |
| Schwefeldioxid (SO2) | Schwefeldioxid ist eine Verbindung aus Schwefel und Sauerstoff, die bei der Verbrennung von Schwefel entsteht. Es spielt eine Rolle in der Luftverschmutzung und wird auch in der Lebensmittelindustrie als Konservierungsmittel verwendet. |
| Ammoniak (NH3) | Ammoniak ist eine Verbindung aus Stickstoff und Wasserstoff. Es wird als Düngemittel, Reinigungsmittel und in der Pharmaindustrie verwendet. |
| Siliciumdioxid (SiO2) | Siliciumdioxid ist eine Verbindung aus Silicium und Sauerstoff, die in Form von Quarz vorkommt. Es wird in der Elektronikindustrie, im Bauwesen und in der Herstellung von Glas verwendet. |
| Schwefelsäure (H2SO4) | Schwefelsäure ist eine starke anorganische Säure, die aus Schwefel, Sauerstoff und Wasserstoff besteht. Sie wird in vielen industriellen Prozessen verwendet, wie z.B. zur Herstellung von Düngemitteln, Batterien und Reinigungsmitteln. |
| Eisenoxid (Fe2O3) | Eisenoxid ist eine Verbindung aus Eisen und Sauerstoff, die in Form von Rost vorkommt. Es wird als Farbstoff und in der Herstellung von Eisenlegierungen verwendet. |
Klassifizierung von anorganischen Stoffen: Metalle und Nichtmetalle
Anorganische Stoffe lassen sich in zwei Hauptkategorien unterteilen: Metalle und Nichtmetalle. Diese Klassifizierung erleichtert das Verständnis der vielfältigen Eigenschaften und Anwendungen anorganischer Materialien.
Metalle zeichnen sich durch ihre gute Leitfähigkeit für Wärme und Elektrizität, Duktilität (Verformbarkeit) und hohe Dichte aus. Typische Beispiele sind Eisen, Kupfer und Aluminium. Metalle bilden oft kristalline Strukturen und sind bekannt für ihre hohe Festigkeit. Sie sind integrale Bestandteile vieler Bauwerke aufgrund ihrer Haltbarkeit und Belastbarkeit.
Nichtmetalle hingegen haben sehr unterschiedliche physikalische und chemische Eigenschaften im Vergleich zu Metallen. Zu den Nichtmetallen gehören berühmte Elemente wie Schwefel, Phosphor und die Edelgase wie Helium und Neon. Diese Substanzen zeigen meist eine schlechte elektrische Leitfähigkeit, sind weniger dicht und nicht verformbar. Ihre Erscheinungsformen reichen von gasförmig bis fest.
Ein weiteres Beispiel sind anorganische Pigmente, welche häufig aus Oxiden oder Sulfiden bestehen. Diese Substanzen werden weitverbreitet zur Herstellung von Farbstoffen verwendet, um dauerhafte, beständige Farben in Kunststoffen, Anstrichen und anderen Materialien zu gewährleisten.
Durch das Verständnis dieser grundlegenden Unterscheidungen zwischen Metallen und Nichtmetallen können wir besser nachvollziehen, warum bestimmte anorganische Substanzen in spezifischen industriellen und wissenschaftlichen Bereichen bevorzugt eingesetzt werden.
Die Kenntnis von Stoffen und deren Eigenschaften bildet die Grundlage aller wissenschaftlichen und industriellen Fortschritte. – Dmitri Mendelejew
| Anorganische Stoffe Beispiele | Eigenschaften und Anwendungen |
|---|---|
| Metalle (z.B. Eisen, Kupfer, Aluminium) | Hohe Leitfähigkeit, Duktilität, verwendet im Bauwesen und der Elektronik |
| Oxide (z.B. Siliziumdioxid, Titanoxid) | Strukturbildend, verwendet in Glas und Keramik |
| Säuren und Basen (z.B. Schwefelsäure, Natriumhydroxid) | Aktiv reagieren, verwendet in der Chemie- und Pharmaindustrie |
| Edelgase (z.B. Helium, Neon) | Geringe Reaktivität, verwendet in Beleuchtung und Kühlung |
| Anorganische Pigmente (z.B. Eisenoxidrot, Titandioxidweiß) | Hohe Beständigkeit, verwendet in Kunststoffen, Farben und Lacken |
Struktur und Eigenschaft anorganischer Verbindungen
Anorganische Verbindungen zeichnen sich durch ihre Vielfalt in Struktur und Eigenschaft aus. Im Gegensatz zu organischen Verbindungen, enthalten anorganische Substanzen keine Kohlenstoff-Wasserstoff-Bindungen. Beispiele für anorganische Stoffe sind Metalle, Minerale, Salze, Säuren und Basen.
Die strukturelle Vielfalt dieser Materialien reicht von einfachen Molekülen bis hin zu komplexen Gitterstrukturen. Metalle wie Eisen oder Kupfer besitzen eine kristalline Struktur, die ihnen hohe Leitfähigkeit und Festigkeit verleiht. Nichtmetalle und Mineralien haben oft deutlich andere Strukturen. Ein bekanntes Beispiel ist Kochsalz (Natriumchlorid), das ein ionisches Gitterbild zeigt.
Eigenschaften wie Härte, Schmelzpunkt und elektrische Leitfähigkeit variieren stark zwischen den unterschiedlichen Typen von anorganischen Verbindungen. Zum Beispiel sind Halogene wie Chlor bei Raumtemperatur gasförmig, während Oxide wie Siliziumdioxid fest sind. Die Ionenverbindungen spielen häufig eine wichtige Rolle in elektrochemischen Anwendungen aufgrund ihrer guten Leitfähigkeit in geschmolzenem oder gelösten Zustand.
Edelgase wie Helium unterscheiden sich durch ihre chemische Inertheit. Ihre volle Elektronenschale macht sie extrem stabil und wenig reaktiv. Erze und anorganische Pigmente finden wiederum vielfältige Verwendung in Industrie und Kunst, da sie dank ihrer stabilen Eigenschaften und oft intensiven Farben besonders begehrt sind.
Um diese Vielfalt zu einem System zusammenzufassen, wird in der Anorganischen Chemie die Einordnung entsprechend der Struktur-Eigenschafts-Beziehung vorgenommen. Dies erleichtert das Verständnis und die gezielte Nutzung anorganischer Materialien in verschiedenen Anwendungsbereichen.
Eigenschaften anorganischer Stoffe
- Meist einfachere Molekülstrukturen als organische Verbindungen.
- Oft höhere Schmelz- und Siedepunkte.
- Viele sind in Wasser löslich, insbesondere Salze.
- Spielen wichtige Rollen in biologischen Systemen, z.B. als Enzym-Aktivatoren oder bei osmotischen Prozessen.
Reaktionen zwischen anorganischen Verbindungen
Reaktionen zwischen anorganischen Stoffen können in verschiedenen Formen auftreten und umfassen eine Vielzahl von Mechanismen. Eine der häufigsten Reaktionsarten ist die Redoxreaktion, bei der Elektronen von einem Reaktanten auf einen anderen übertragen werden. Beispielsweise reagieren Metalle wie Eisen oft mit Sauerstoff zu Metalloxiden, ein Prozess, der allgemein als Rostbildung bekannt ist.
Ein weiteres Beispiel sind Säure-Base-Reaktionen, bei denen eine Säure mit einer Base reagiert, um Wasser und ein Salz zu bilden. Ein klassisches Experiment hierfür ist die Reaktion von Salzsäure (HCl) mit Natriumhydroxid (NaOH), wobei Wasser (H2O) und Natriumchlorid (NaCl) entstehen.
Thermodynamik spielt eine wichtige Rolle beim Verständnis dieser Reaktionen. Faktoren wie Temperatur und Druck können das Gleichgewicht und die Geschwindigkeit dieser chemischen Vorgänge erheblich beeinflussen. Zum Beispiel beschleunigt eine höhere Temperatur viele Reaktionen, während andere durch Drucksteigerung begünstigt werden.
Auch Ligandenaustauschreaktionen sind häufig in der Anorganischen Chemie anzutreffen. Dabei tauscht ein Komplex-Ion seine gebundenen Liganden gegen unterschiedliche Moleküle oder Ionen aus, was insbesondere für Übergangsmetallkomplexe relevant ist.
In industriellen Anwendungen werden viele dieser Reaktionen genutzt, um wertvolle chemische Verbindungen ohne Kohlenstoff herzustellen, sei es in Form von Salzen, Oxiden, oder anderen anorganischen Materialien. So dient die Umsetzung von Kalk (Calciumcarbonat) zu Calciumoxid und Kohlendioxid beispielsweise zur Herstellung von Zement, einem wesentlichen Baustoff.
Die anorganische Chemie umfasst etwa 50.000 bekannte chemische Verbindungen und ist damit deutlich kleiner als das Gebiet der organischen Chemie. Dennoch sind anorganische Stoffe von fundamentaler Bedeutung für das Leben und viele technische Anwendungen.
Verwendung in Bauwesen und Medizin
Anorganische Stoffe haben zahlreiche Anwendungen im Bauwesen und in der Medizin. Beton beispielsweise, das wohl am meisten verwendete Baumaterial weltweit, besteht hauptsächlich aus anorganischen Verbindungen wie Zement und Sand, die zu robusten und langlebigen Bauten führen.
Auch Stahl, eine Legierung aus Eisen und Kohlenstoff, enthält anorganische Anteile und wird häufig aufgrund seiner Festigkeit und Flexibilität im Hoch- und Tiefbau eingesetzt. Beton und Stahl sind nur zwei Beispiele für anorganische Materialien im Bauwesen, aber auch andere Metalle wie Aluminium und Kupfer finden hier Anwendung.
In der Medizin spielen Anorganische Substanzen ebenfalls eine wichtige Rolle. Zum Beispiel werden Calciumphosphate zur Reparatur von Knochenbrüchen und als Bestandteil von Zahnfüllungen verwendet.
Außerdem kommen anorganische Stoffe wie Titaniumdioxid in Zahnpasten zum Einsatz, um Abriebfestigkeit und antibakterielle Eigenschaften zu verbessern.
Ein weiteres anorganisches Material in der Medizin ist Silbernitrat, das wegen seiner antiseptischen Eigenschaften als Desinfektionsmittel gebraucht wird. Diese Anwendungen zeigen, wie entscheidend anorganische Chemie in verschiedenen Bereichen des täglichen Lebens ist und wie sie unsere moderne Gesellschaft mitprägt.
Von Baustoffen bis hin zu medizinischen Applikationen bieten anorganische Materialien unverzichtbare Lösungen für viele Branchen.
Video: Erklärvideo Anorganische Stoffe
Video-Link: https://www.youtube.com/watch?v=sg9fvZfYbsI
| Stoffkategorie | Beispiele | Hauptanwendung |
|---|---|---|
| Metalle | Eisen, Kupfer, Aluminium | Bauwesen, Elektronik |
| Oxide | Siliziumdioxid, Titanoxid | Glas, Keramik |
| Säuren und Basen | Schwefelsäure, Natriumhydroxid | Chemie-, Pharmaindustrie |
| Edelgase | Helium, Neon | Beleuchtung, Kühlung |
| Anorganische Pigmente | Eisenoxidrot, Titandioxidweiß | Kunststoffe, Farben, Lacke |
Katalysator- und Halbleiteranwendungen
Anorganische Stoffe spielen eine entscheidende Rolle in Katalysator- und Halbleiteranwendungen. Viele industrielle Prozesse basieren auf der Verwendung von Katalysatoren, die chemische Reaktionen beschleunigen, ohne dabei selbst verbraucht zu werden. Ein bekanntes Beispiel ist die Nutzung von Platin in der Automobilindustrie zur Reduktion von Schadstoffen im Abgas.
Auch in der Chemie finden anorganische Katalysatoren breite Anwendung. Beispielsweise wird Eisen in der Ammoniaksynthese nach dem Haber-Bosch-Verfahren eingesetzt. Hierbei wird Stickstoff aus der Luft mit Wasserstoff zu Ammoniak umgesetzt, einem wichtigen Ausgangsstoff für Düngemittel.
In der Elektronik und Informationstechnologie sind anorganische Materialien unersetzlich. Silizium, ein Element der Gruppe der Halbmetalle, bildet die Grundlage für die Produktion von Halbleitern. Diese Halbleiter sind das Herzstück moderner Elektronikgeräte wie Computerchips und Solarzellen.
Ebenso werden Verbindungen wie Galliumarsenid (GaAs) und Indiumphosphid (InP) verwendet, um effizientere Halbleiter herzustellen. Sie bieten eine höhere Leistung und schnellere Verarbeitungsgeschwindigkeiten als herkömmliches Silizium.
Zusammengefasst: Die verschiedenen Anwendungen von anorganischen Stoffen in Katalyse- und Halbleitersystemen demonstrieren eindrucksvoll ihre Vielseitigkeit und Bedeutung für technische und industrielle Entwicklungen.
Umweltfreundliche anorganische Materialien
Die Entwicklung umweltfreundlicher anorganischer Materialien gewinnt zunehmend an Bedeutung. Diese Materialien zeichnen sich durch ihre geringe Umweltbelastung und nachhaltige Produktion aus. Beispiele für solche Materialien sind bestimmte Arten von Oxiden, die in Solarzellen verwendet werden, oder Metalle wie Aluminium und Titan, die aufgrund ihrer Recyclingfähigkeit geschätzt werden.
Minerale und Ionenverbindungen finden ebenso Anwendung in der grünen Technologie, wie z.B. bei der Reinigung von Wasser oder der Abscheidung von CO2. Hierbei handelt es sich oftmals um innovative Lösungen, die helfen, Ressourcen zu schonen und Schadstoffe zu reduzieren.
Salze und Säuren können ebenfalls umweltfreundlich eingesetzt werden. Zum Beispiel bietet die Verwendung von Magnesiumsulfat eine effektive Möglichkeit zur Verbesserung der Bodenqualität ohne den Einsatz von künstlichen Düngemitteln. Dies zeigt, dass auch traditionelle anorganische Substanzen nachhaltig genutzt werden können.
Ein weiteres Beispiel stellt der Einsatz von Edelgasen wie Argon in energieeffizienten Beleuchtungssystemen dar. Diese Gase haben den Vorteil, nicht mit anderen Stoffen zu reagieren und somit keine schädlichen Nebenprodukte zu erzeugen. Dies macht sie ideal für Anwendungen, die sowohl langlebig als auch umweltverträglich sein müssen.
Anorganische Pigmente wiederum bieten Möglichkeiten zur Herstellung umweltfreundlicher Farben und Lacke. Sie enthalten keine organischen Lösungsmittel, was die Emission von flüchtigen organischen Verbindungen (VOCs) reduziert.
Zusammenfassend kann gesagt werden, dass die Forschung und Anwendung umweltfreundlicher anorganischer Materialien entscheidend ist, um eine nachhaltigere Zukunft zu gestalten.