Oxidationsmittel einfach erklärt: Definition & Beispiele
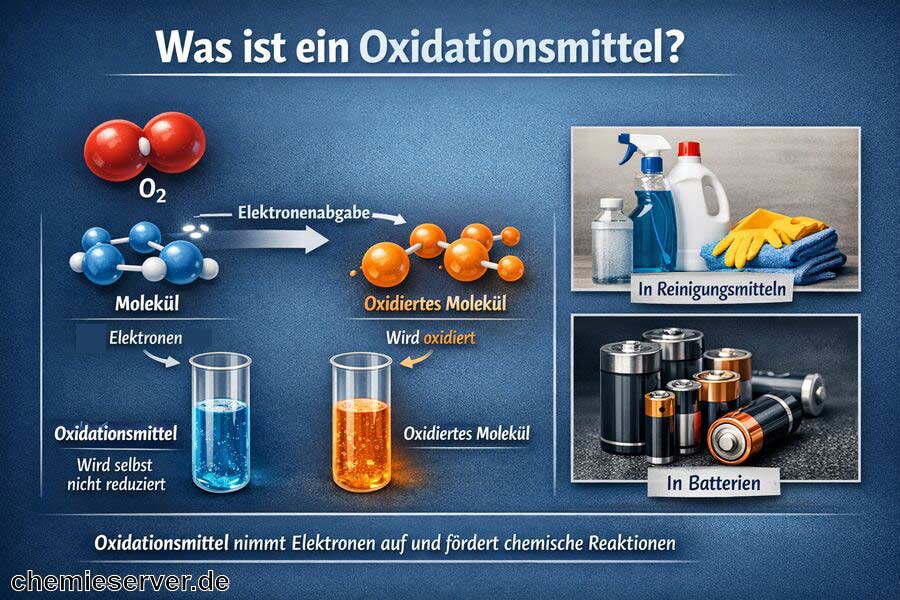
Ein Oxidationsmittel ist eine Substanz, die in chemischen Reaktionen Elektronen von anderen Teilchen aufnimmt. Dabei wird das Oxidationsmittel selbst reduziert und bewirkt gleichzeitig die Oxidation des Reaktionspartners. Solche Stoffe werden häufig in Reinigungsmitteln, Batterien und technischen Prozessen eingesetzt, da ihre Elektronenaufnahme chemische Umwandlungen ermöglicht. Durch diese Reaktionen verändern sich die Eigenschaften der beteiligten Stoffe oft deutlich.
In chemischen Reaktionsabläufen steuern Oxidationsmittel den Verlauf entscheidend, indem sie gezielt andere Stoffe oxidieren. Dadurch spielen sie eine wichtige Rolle bei Reinigungsprozessen, der Energiegewinnung und vielen weiteren Anwendungen.
Wichtiges am Anfang
- Oxidationsmittel nehmen Elektronen von anderen Molekülen auf, wodurch diese oxidiert werden.
- Sie werden selbst reduziert und wirken als Elektronenakzeptoren in chemischen Reaktionen.
- Oxidationsmittel oxidieren andere Stoffe, indem sie Elektronen aufnehmen.
- Sie werden in Reinigung, Batterien und chemischen Prozessen vielfältig eingesetzt.
- Ihre Wirkung basiert auf der Fähigkeit, durch Elektronenaufnahme chemische Veränderungen zu bewirken.
| Merkmal | Beschreibung | Beispiele | Anwendungsbereiche |
|---|---|---|---|
| Elektronenübertragung | Oxidationsmittel nehmen Elektronen von anderen Molekülen auf | Wasserstoffperoxid, Sauerstoff | Reinigungsmittel, Batterien |
| Funktion als Oxidator | Werden selbst reduziert und oxidieren andere Stoffe | Chlor, Kaliumpermanganat | Chemische Synthesen, Desinfektion |
| Funktion | Elektronenaufnahme führt zu chemischen Veränderungen der Reaktionspartner | Oxidation von Metallen, Reinigungsprozesse | Industrielle Produktion, Reinigung |
| Merkmale | Nimmt Elektronen auf, wirkt als Oxidator, beeinflusst Reaktionen maßgeblich | Chlorbleiche, Bleichmittel | Haushalt, Industrie |
Substanz, die Elektronen auf andere Moleküle überträgt
Ein Oxidationsmittel ist eine Substanz, die in chemischen Reaktionen als Elektronenakzeptor wirkt. Dabei nimmt sie Elektronen von anderen Atomen oder Molekülen auf und verändert so deren chemischen Zustand. Durch diesen Vorgang wird das Oxidationsmittel selbst reduziert, während die Reaktionspartner oxidiert werden. Dadurch können chemische Bindungen leichter umgewandelt oder aufgebrochen werden.
Diese Eigenschaft macht Oxidationsmittel zu einem zentralen Bestandteil vieler chemischer Prozesse. Sie ermöglichen unter anderem die Zersetzung von Schadstoffen bei Reinigungsprozessen oder den Ablauf energieumsetzender Reaktionen in Batterien. Durch die gezielte Elektronenaufnahme steuern Oxidationsmittel chemische Umwandlungen und sind daher in zahlreichen industriellen und technischen Anwendungen unverzichtbar.
Verursacht Selbstoxidation in Reaktionen
In chemischen Reaktionen wird ein Oxidationsmittel selbst reduziert, das heißt, es nimmt Elektronen auf und verändert dabei seinen Oxidationszustand. Dieses Verhalten ist typisch für Stoffe, die als Elektronenakzeptoren wirken. Während sie anderen Teilchen Elektronen entziehen und diese dadurch oxidieren, erfährt das Oxidationsmittel selbst eine chemische Veränderung durch die Elektronenaufnahme. In vielen Fällen kann es nach der Reaktion erneut oxidiert werden und so wieder in einen höheren Oxidationszustand übergehen.
Typische Beispiele sind Kaliumpermanganat oder Chlor, deren chemische Struktur sich bei Reaktionen verändert, weil sie Elektronen aufnehmen. Solche Prozesse sind in zahlreichen Anwendungen von Bedeutung, etwa bei Reinigungs- und Desinfektionsmitteln, bei denen die Reduktion des Oxidationsmittels direkt mit der Wirksamkeit zusammenhängt. Die Fähigkeit bestimmter Stoffe, sich selbst reduzieren zu lassen, ist daher entscheidend für viele chemische Abläufe und trägt wesentlich zur Effizienz technischer und industrieller Verfahren bei.
„Die Fähigkeit eines Stoffes, Elektronen aufzunehmen, bestimmt seine Rolle in der Chemie und beeinflusst maßgeblich die Natur der Reaktionen.“ – Gilbert Lewis
Nimmt Elektronen auf, wird reduziert – wirkt als Oxidator
Ein Oxidationsmittel ist dadurch gekennzeichnet, dass es in chemischen Reaktionen Elektronen aufnimmt und dabei selbst reduziert wird. Es wirkt als Oxidator, da es anderen Stoffen Elektronen entzieht und diese dadurch oxidiert. Im Gegensatz dazu geben Reduktionsmittel Elektronen ab und werden selbst oxidiert. Durch seine Funktion als Elektronenakzeptor ermöglicht das Oxidationsmittel gezielte Redoxreaktionen und spielt eine zentrale Rolle bei der Steuerung chemischer Prozesse.
Die Eigenschaft, selbst reduziert zu werden, erlaubt in vielen Fällen eine Regeneration des Oxidationsmittels. Nach der Reduktion kann es erneut oxidiert werden und bleibt damit reaktionsfähig. Diese Eigenschaft ist besonders wichtig für industrielle Anwendungen wie Bleichen, Reinigungsprozesse oder den Abbau von Schadstoffen. Die Wirkung beruht stets auf der Fähigkeit, Elektronen aufzunehmen und dadurch chemische Umwandlungen auszulösen.
Einsatz von Oxidationsmitteln in chemischen Reaktionen
Oxidationsmittel werden in zahlreichen chemischen Reaktionen eingesetzt, um Stoffe gezielt zu oxidieren. In industriellen Verfahren ermöglichen sie die Umwandlung von Rohstoffen und Zwischenprodukten und machen viele Produktionsschritte erst möglich. Auch im Alltag finden sie Anwendung, etwa in Reinigungsmitteln oder beim Bleichen von Textilien, wo Verschmutzungen durch Oxidation abgebaut werden.
Ein weiterer wichtiger Bereich ist die Energieumwandlung, zum Beispiel in Batterien, bei denen Oxidationsmittel an kontrollierten Redoxreaktionen beteiligt sind. Auch in der Lebensmittelverarbeitung werden sie eingesetzt, um Haltbarkeit und Qualität zu verbessern. Ihre Vielseitigkeit macht sie zu einem festen Bestandteil moderner Technik und Chemie.
Führt zur Oxidation der Reaktionspartner
Durch die Elektronenaufnahme des Oxidationsmittels werden die beteiligten Reaktionspartner oxidiert. Dabei verändern sich deren chemische Eigenschaften, was sich etwa in Strukturänderungen, Farbveränderungen oder neuen Stoffeigenschaften zeigt. Beispiele sind Korrosionsprozesse bei Metallen oder der Abbau organischer Verbindungen.
Diese gezielte Oxidation wird in vielen technischen und industriellen Anwendungen genutzt, etwa zur Desinfektion, zur Reinigung von Oberflächen oder zur Energiegewinnung. Die Fähigkeit von Oxidationsmitteln, andere Stoffe zu oxidieren, bildet die Grundlage zahlreicher chemischer Verfahren und ermöglicht eine gezielte Steuerung chemischer Veränderungen.
Häufig in Reinigungsmitteln und Batterien verwendet
Oxidationsmittel finden häufig Anwendung in Reinigungsmitteln, da sie durch ihre Fähigkeit, Schmutz und Schadstoffe zu oxidieren, Oberflächen wirkungsvoll säubern. Besonders Substanzen wie Kaliumpermanganat oder Chlorbleiche werden gezielt eingesetzt, um Flecken, Keime und organische Rückstände zu beseitigen. Durch denoxidierende Effekt können sie Verschmutzungen auf chemischer Ebene lösen, was das Reinigen deutlich erleichtert und beschleunigt. Zudem sorgen sie dafür, dass Bakterien und Viren abgetötet werden, wodurch die Desinfektion unterstützt wird.
In Batterien spielt das Oxidationsmittel eine ebenso zentrale Rolle. Hier ermöglichen es Redoxreaktionen, elektrische Energie zu gewinnen. Beispielsweise sind in vielen Akkus substanzielle Bestandteile wie Sauerstoff oder andere elektronenakzeptierende Verbindungen enthalten, die während des Lade- und Entladevorgangs Elektronen aufnehmen oder abgeben. Diese Vorgänge steuern den Energiefluss und liefern somit die Grundlage für den Betrieb verschiedener elektrischer Geräte. Der Einsatz solcher Stoffe sorgt zudem für eine stabile Struktur der Batterie und trägt dazu bei, die Spannung konstant zu halten.
In beiden Anwendungsfeldern ist die Fähigkeit eines Oxidationsmittels, chemisch Reaktionen gezielt zu beeinflussen, grundlegend. Bei der Reinigung geht es vor allem um die Entfernung von Verschmutzungen, während in Batterien die Umwandlung chemischer Energie in elektrische Energie im Vordergrund steht. Diese vielseitige Nutzung macht sie zu einem wichtigen Bestandteil vieler technischer Produkte, die im Alltag regelmäßig verwendet werden.