Die wichtigsten chemischen Fachbegriffe für Anfänger
In der Chemie gibt es eine Vielzahl von Fachbegriffen, die das Verständnis komplexer Prozesse erleichtern und präzise Kommunikation ermöglichen. Zu den grundlegenden Begriffen zählen Atom, Molekül sowie Element und Verbindung. Diese Begriffe bilden die Basis, um chemische Strukturen und Reaktionen klar zu beschreiben. Darüber hinaus sind Kenntnisse über Säure und Base wichtig, da sie zentrale Rollen in zahlreichen chemischen Reaktionen spielen. Das Verstehen dieser Konzepte liefert Einblicke in die Funktion und den Aufbau verschiedener Stoffe. Ein umfassendes Wissen um diese Fachbegriffe ermöglicht es, chemische Vorgänge verständlich darzustellen und dient als Grundlage für weiterführende Studien oder praktische Anwendungen.
Wichtiges am Anfang
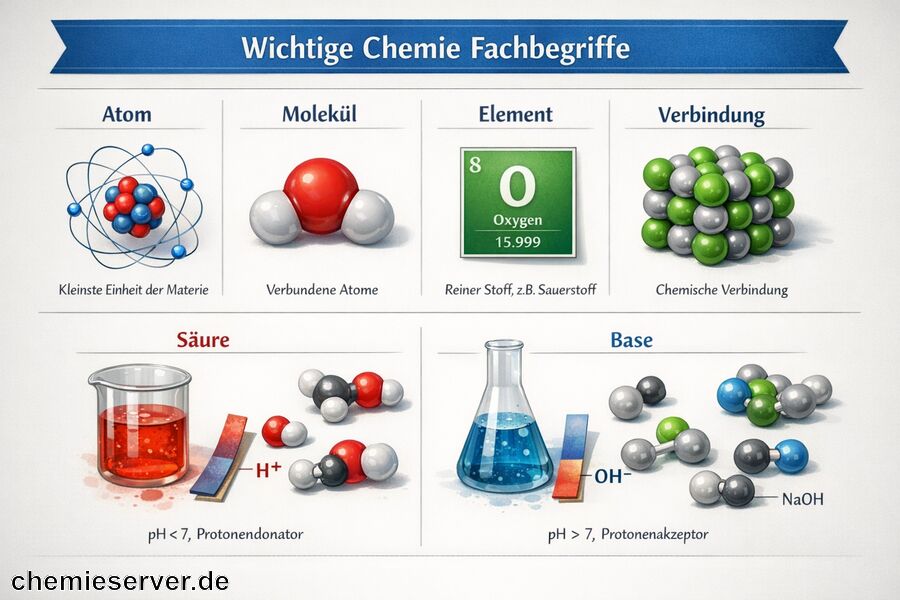
- Ein Atom ist die kleinste Einheit eines Elements mit eigenständigen chemischen Eigenschaften.
- Moleküle bestehen aus mehreren Atomen, die durch chemische Bindungen verbunden sind.
- Elemente bestehen nur aus einer Atomart; Verbindungen enthalten mindestens zwei verschiedene Elemente.
- Säuren und Basen sind wichtige Stoffgruppen, die in chemischen Reaktionen eine zentrale Rolle spielen.
- Reaktionen beinhalten den Austausch oder die Neuordnung von Atomen, um neue Stoffe zu bilden.
Atom, Molekül, Reaktion, Element, Verbindung, Säure, Base
Ein Atom ist die kleinste Einheit eines chemischen Elements und besitzt alle charakteristischen Eigenschaften dieses Elements. Es besteht aus einem Kern, der Protonen und Neutronen enthält, sowie einer Elektronenhülle, in der die Elektronen angeordnet sind. Atome sind die Bausteine für größere Strukturen in der Chemie.
Mehrere Atome können sich zu einem Molekül verbinden. Dabei handelt es sich um die kleinste Einheit eines chemischen Stoffes, die noch alle Eigenschaften des Stoffes aufweist. Moleküle entstehen durch chemische Bindungen zwischen den Atomen, was ihre Stabilität und Reaktionsfähigkeit beeinflusst.
Bei einer Chemischen Reaktion ändern sich die Verbindungen, indem Atome neu angeordnet oder chemisch gebunden werden. Dabei werden Energie verändert, und es können neue Stoffe entstehen. Das Verständnis von Reaktionen ist grundlegend, um Prozesse in der Natur und Technik nachvollziehen zu können.
Ein Element beschreibt eine reine Stoffart, die nur aus einer Art von Atomen besteht. Beispiele hierfür sind Wasserstoff (H) oder Sauerstoff (O). Elemente bilden die Grundlage aller chemischer Verbindungen und werden im Periodensystem systematisch dargestellt.
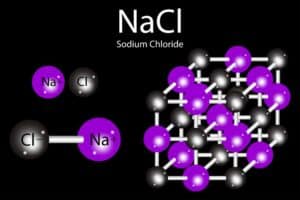
Im Gegensatz dazu steht die Verbindung, die aus mindestens zwei unterschiedlichen Elementen besteht, wie Salz (NaCl). Diese Stoffe verfügen über eigene Eigenschaften und unterscheiden sich deutlich von reinen Elementen.
Ein weiteres zentrales Konzept sind Säuren und Basen. Säuren sind Substanzen, die in Wasser H⁺-Ionen freisetzen, während Basen Hydroxidionen (OH⁻) enthalten und in der Lage sind, H⁺-Ionen zu binden. Zusammen regeln sie viele wichtige Prozesse in der Chemie, Biologie und Medizin.
| Begriff | Definition | Beispiel | Wichtigkeit |
|---|---|---|---|
| Atom | Die kleinste Einheit eines Elements, die die chemischen Eigenschaften besitzt. | Wasserstoffatom | Grundbaustein der Materie |
| Molekül | Eine Verbindung aus zwei oder mehreren Atomen, die chemisch miteinander verbunden sind. | Wassermolekül (H₂O) | Zentrale Rolle bei chemischen Reaktionen |
| Element | Eine Substanz, die nur aus einer Art von Atomen besteht. | Gold (Au), Sauerstoff (O) | Basis der chemischen Vielfalt |
| Verbindung | Eine Substanz, die aus zwei oder mehr verschiedenen Elementen besteht. | Salz (NaCl) | Unterscheidet sich vom reinen Element |
Weitere wichtige chemische Fachbegriffe
Kernbegriffe
- Aggregatzustand: Der Aggregatzustand beschreibt, ob ein Stoff fest, flüssig oder gasförmig vorliegt, und bestimmt dadurch grundlegende Eigenschaften wie Dichte, Form und Volumen.
- Bindung (chemisch): Eine chemische Bindung ist die Kraft, die Atome zusammenhält, etwa in kovalenten, ionischen oder metallischen Bindungen, und so die Bildung von Molekülen ermöglicht.
- Katalysator: Ein Katalysator ist eine Substanz, die eine chemische Reaktion beschleunigt, ohne dabei selbst verbraucht oder dauerhaft verändert zu werden.
- pH-Wert: Der pH-Wert ist ein Maß für die Stärke von Säuren und Basen auf einer Skala von 0 bis 14, wobei Werte unter 7 sauer und Werte über 7 basisch sind.
- Redox-Reaktion: Eine Redox-Reaktion ist eine chemische Reaktion, bei der Elektronen übertragen werden, wobei Oxidation die Abgabe und Reduktion die Aufnahme von Elektronen bezeichnet.
Analytik und Stoffe
- Lösung: Eine Lösung ist ein homogenes Gemisch, bei dem ein Stoff gleichmäßig in einem Lösungsmittel verteilt ist, wie zum Beispiel Zucker in Wasser.
- Gemisch: Ein Gemisch besteht aus mehreren Stoffen, die nicht chemisch miteinander verbunden sind und daher ohne chemische Reaktion getrennt werden können.
- Isotop: Isotope sind Atome desselben Elements, die sich durch eine unterschiedliche Anzahl an Neutronen im Atomkern unterscheiden.
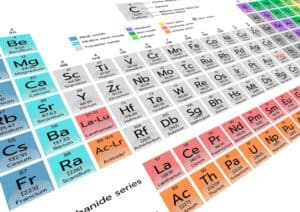
- Periodensystem: Das Periodensystem ist eine geordnete Übersicht aller chemischen Elemente nach ihrer Protonenzahl und zeigt wichtige Zusammenhänge wie Reaktivität und chemische Eigenschaften.
- Funktionelle Gruppe: Eine funktionelle Gruppe ist ein bestimmter Teil eines Moleküls, der maßgeblich dessen chemische Eigenschaften und Reaktionsverhalten bestimmt.
Stoffeigenschaften
- Dichte: Die Dichte beschreibt das Verhältnis von Masse zu Volumen und ist eine charakteristische Eigenschaft eines Stoffes bei einer bestimmten Temperatur.
- Schmelzpunkt / Siedepunkt: Der Schmelzpunkt ist die Temperatur, bei der ein Stoff vom festen in den flüssigen Zustand übergeht, während der Siedepunkt den Übergang vom flüssigen in den gasförmigen Zustand kennzeichnet.
- Löslichkeit: Die Löslichkeit gibt an, wie gut sich ein Stoff in einem bestimmten Lösungsmittel lösen kann und hängt von Temperatur und Stoffart ab.
Reaktionsarten
- Ausfällungsreaktion: Bei einer Ausfällungsreaktion entsteht aus einer Lösung ein unlöslicher Feststoff, der als Niederschlag sichtbar wird.
- Neutralisation: Eine Neutralisation ist eine Reaktion zwischen einer Säure und einer Base, bei der Salz und Wasser entstehen und sich der pH-Wert ausgleicht.
- Verbrennung: Eine Verbrennung ist eine chemische Reaktion eines Stoffes mit Sauerstoff, die meist exotherm verläuft und häufig Kohlendioxid und Wasser als Produkte liefert.
Messgrößen
- Molare Masse: Die molare Masse gibt die Masse eines Mols, also von 6,022×10²³ Teilchen, eines Stoffes in Gramm pro Mol an.
- Konzentration: Die Konzentration beschreibt die Menge einer gelösten Substanz bezogen auf ein bestimmtes Volumen, häufig angegeben in Mol pro Liter.
- Chemisches Gleichgewicht: Ein chemisches Gleichgewicht liegt vor, wenn eine umkehrbare Reaktion abläuft und sich die Stoffmengen der beteiligten Substanzen nicht mehr ändern.
Organische Chemie
- Isomerie: Isomerie bezeichnet das Phänomen, dass Verbindungen die gleiche Summenformel besitzen, sich aber in ihrer Struktur oder räumlichen Anordnung unterscheiden.
- Polymer: Ein Polymer ist ein großes Molekül, das aus vielen miteinander verknüpften Bausteinen, den Monomeren, besteht, wie es bei Kunststoffen der Fall ist.