Chiralität und Enantiomerie sind fundamentale Konzepte in der organischen Chemie. Diese behandeln die Händigkeit von Molekülen, was sich auf deren Fähigkeit bezieht, Spiegelbilder zu formen, die nicht deckungsgleich sind. Solche spiegelbildlichen Formen werden als Enantiomere bezeichnet. Enantiomere besitzen identische chemische Eigenschaften, unterscheiden sich jedoch in der Art und Weise, wie sie mit polarisiertem Licht interagieren, ein Phänomen, das als Optische Isomerie bekannt ist.
Die charakteristische Eigenschaft chiraler Moleküle, ihre molekulare Asymmetrie, spielt eine kritische Rolle sowohl in natürlichen biologischen Prozessen als auch in synthetischen Anwendungen. Die Bestimmung der absoluten Konfiguration einer Verbindung ist ausschlaggebend für das Verständnis ihrer biologischen Aktivität. In vielen Fällen kann ein Gemisch aus gleichen Mengen zweier Enantiomeren–bekannt als racemische Gemische–getrennt werden, um spezifische Wirkungen zu erzielen.
Das Wichtigste in Kürze
- Chiralität entsteht durch asymmetrische Kohlenstoffatome, wodurch spiegelbildliche, nicht deckungsgleiche Moleküle, sogenannte Enantiomere, gebildet werden.
- Enantiomere haben identische physikalische Eigenschaften, unterscheiden sich jedoch in der optischen Aktivität und biologischen Wirkung.
- Racemische Gemische enthalten gleiche Mengen beider Enantiomere und zeigen keine optische Aktivität.
- Die Trennung von Enantiomeren erfolgt durch Techniken wie chromatographische Methoden und Kristallisation.
- Chiralität ist entscheidend in der Pharmazie, da unterschiedliche Enantiomere verschiedene therapeutische Wirkungen haben können.
Chiralität bezieht sich auf die Eigenschaft eines Moleküls, nicht mit seinem Spiegelbild identisch zu sein. Enantiomerie bezeichnet das Phänomen, dass chirale Moleküle (Enantiomere) zueinander spiegelbildlich sind und sich in ihrer räumlichen Anordnung der Atome unterscheiden. Enantiomere besitzen die gleiche chemische Struktur, aber können unterschiedliche biologische Aktivitäten oder pharmakologische Eigenschaften aufweisen.
Beispiele
- Ein bekanntes Beispiel für chirale Moleküle sind die Enantiomere von Limonen, einem Bestandteil von Zitrusfrüchten. Sie unterscheiden sich in ihrer räumlichen Anordnung und verleihen daher unterschiedliche Gerüche.
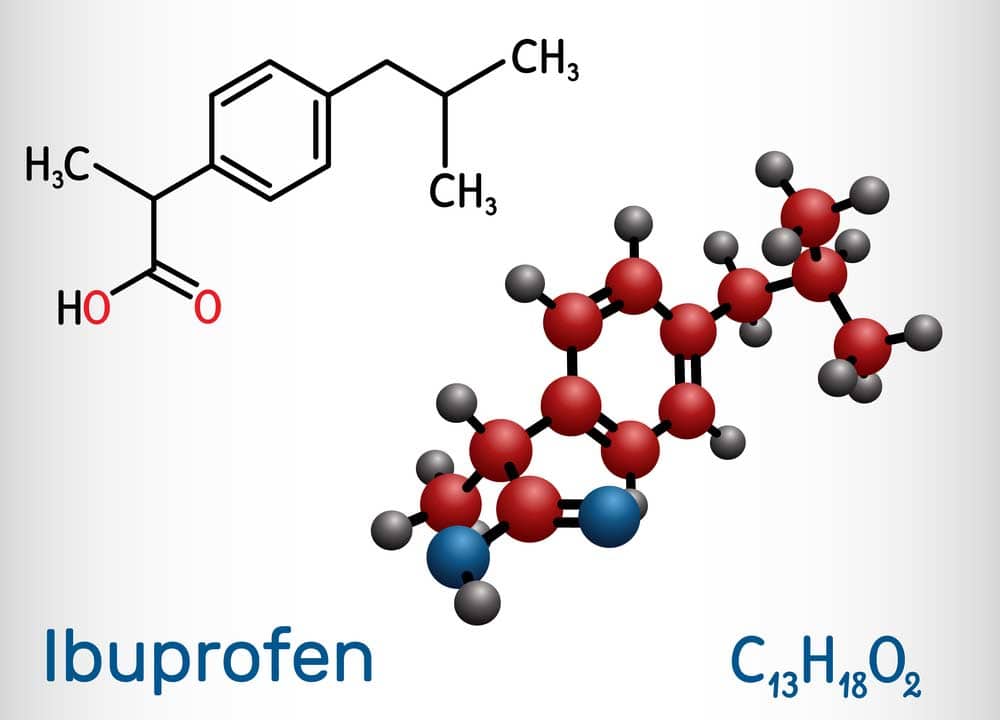
- Ein weiteres Beispiel sind die Enantiomere von Ibuprofen, einem schmerzstillenden Medikament. Das (S)-Ibuprofen ist wirksamer als das (R)-Ibuprofen.
- Auch Aminosäuren wie L-Alanin und D-Alanin sind Enantiomere und spielen eine wichtige Rolle in der Biochemie.
- Die Enantiomere von Carvon sind verantwortlich für den charakteristischen Geruch von Kümmel bzw. Minze.
- Die beiden Enantiomere von Thalidomid haben unterschiedliche pharmakologische Eigenschaften, was zu tragischen Folgen in der Medizingeschichte führte.
- Die Enantiomere von Propofol, einem Narkosemittel, zeigen unterschiedliche pharmakokinetische Eigenschaften im menschlichen Körper.
Entstehung der Chiralität in organischen Verbindungen
Chiralität in organischen Verbindungen entsteht durch das Vorhandensein eines asymmetrischen Kohlenstoffatoms. Ein solches Kohlenstoffatom ist an vier verschiedene Substituenten gebunden, was zu einer molekularen Asymmetrie führt. Diese asymmetrische Struktur bedeutet, dass das Molekül und sein Spiegelbild nicht identisch sind – ähnlich wie die rechte und linke Hand, eine Eigenschaft, die als Händigkeit von Molekülen bekannt ist.
Die molekulare Chiralität wird oft in Kombination mit dem Konzept der optischen Isomerie untersucht. Jedes chirale Zentrum kann zwei Konfigurationen einnehmen, die sich zueinander wie Bild und Spiegelbild verhalten. Diese Konfigurationen werden Enantiomere genannt. Die unterschiedliche räumliche Anordnung ihrer Atome führt dazu, dass Enantiomerenpaare unterschiedliche biologische und chemische Eigenschaften haben können.
Der Begriff „Absolute Konfiguration“ bezeichnet die genaue dreidimensionale Anordnung der Atome um das chirale Zentrum. Methoden zur Bestimmung dieser Konfiguration umfassen unter anderem Röntgenkristallographie und moderne spektroskopische Techniken. Diese Absolute Konfiguration ist entscheidend für das Verständnis geomtrischer Strukturen und deren Reaktionen.
Zusammenfassend lässt sich sagen, dass die Entstehung der Chiralität und Enantiomerie auf einem komplexen Zusammenspiel zwischen atomaren Bindungen und räumlicher Anordnung basiert. Dieses Phänomen hat weitreichende Implikationen in Bereichen wie Pharmazie und Chemie.
Die Chiralität ist einer der grundlegendsten Aspekte der Chemie, der die Einzigartigkeit und Vielfalt organischer Moleküle erklärt.
– Vladimir Prelog
| Eigenschaft | Enantiomere |
|---|---|
| Chirales Zentrum | Mindestens ein asymmetrisches Kohlenstoffatom |
| Absolute Konfiguration | Unterschiedlich (R- oder S-Form) |
| Physikalische Eigenschaften | Identisch außer der Wechselwirkung mit polarisiertem Licht |
| Biologische Aktivität | Oft sehr unterschiedlich |
| Reaktion mit anderen chiralen Molekülen | Enantioselektiv |
Definition und Eigenschaften von Enantiomeren
In der organischen Chemie versteht man unter Enantiomeren Paare von Molekülen, die spiegelbildlich zueinander sind und sich nicht zur Deckung bringen lassen. Diese Eigenschaft wird auch als Händigkeit von Molekülen bezeichnet, da sie wie linke und rechte Hände erscheinen. Enantiomere haben identische physikalische und chemische Eigenschaften in einer achiralen Umgebung, unterscheiden sich jedoch in ihrem Verhalten gegenüber polarisiertem Licht und bei Reaktionen mit anderen chiralen Verbindungen.
Ein wesentliches Merkmal von Enantiomeren ist ihre optische Aktivität. Wenn eine Lösung eines Enantiomers durch einen Polarisator untersucht wird, dreht das Enantiomer die Ebene des polarisierten Lichts entweder nach rechts (dextrorotatorisch) oder nach links (levorotatorisch). Der Winkel dieser Drehung kann mithilfe der Polarimetrie gemessen werden, was Rückschlüsse auf die Konzentration und Reinheit eines Enantiomers ermöglicht.
Die spezifische Anordnung der Atome in einem Enantiomer wird als seine absolute Konfiguration bezeichnet und durch R- bzw. S-Nomenklatur beschrieben. Obwohl Enantiomere in vielen Aspekten identisch sind, zeigen sie deutlich unterschiedliche biologische Aktivitäten. Dieser Unterschied kommt besonders in der Pharmazie zum Tragen, wo ein Enantiomer eines Arzneimittels therapeutisch wirksam sein kann, während sein Spiegelbildisomer ineffektiv oder sogar schädlich ist. Daher spielt die enantioselektive Synthese eine entscheidende Rolle in der Medikamentenherstellung.
Racemische Gemische und Separationsmethoden
Racemische Gemische oder Razemate sind Mischungen, die aus gleichen Mengen der beiden Enantiomeren einer chiralen Verbindung bestehen. Diese Gemische zeigen keine optische Aktivität, da sich die Drehung des polarisierten Lichts durch die eine Form stets gegenseitig mit der anderen aufhebt.
Die Trennung solcher Gemische in ihre einzelnen Enantiomere ist in vielerlei Hinsicht von großer Bedeutung. Dabei gibt es verschiedene Methoden zur Chiralen Trennung. Eine häufig eingesetzte Technik ist die Kristallisation – hier nutzt man die unterschiedliche Löslichkeit der beiden Enantiomere in einem Lösungsmittel aus.
Eine andere effektive Methode stellt die enantioselektive Chromatographie dar. Hierbei werden spezielle Säulen verwendet, die unterschiedlich starke Wechselwirkungen mit den beiden Enantiomeren haben und sie somit trennen können. Auch enzymatische Methoden spielen eine Rolle; dabei katalysieren Enzyme spezifisch nur ein Enantiomer, was dessen Trennung erleichtert.
Durch moderne Technologien wie die Hochleistungsflüssigkeitschromatographie (HPLC) und Gaschromatographie (GC) wird die Trennung rassimischer Gemische präziser und effektiver gestaltet. Ziel ist es hierbei, möglichst hohe Reinheitsgrade zu erzielen, um chirale Verbindungen für Anwendungen in Pharmazie und Medizin bereitzustellen.
Optische Aktivität und Polarimetrie
Die optische Aktivität ist eine Eigenschaft chiraler Moleküle, die es ihnen ermöglicht, die Ebene des polarisierten Lichts zu drehen. Diese Drehung kann mit einem speziellen Instrument, dem Polarimeter, gemessen werden. Ein Polarimeter besteht aus einer Lichtquelle, einem Polarisationsfilter und einem Detektor.
Wenn ein Lösungsmittel durch das Polarimeter fließt, rotiert das Licht um einen spezifischen Winkel, der als optische Drehung bezeichnet wird. Der Betrag dieser Drehung hängt von der Konzentration der chiralen Substanz und der Weglänge ab, durch die das Licht hindurchtreten muss. Die Einheit der Messung dieser Rotation ist Grad (°).
Optische Isomerie, auch bekannt als Spiegelbildisomerie, spielt eine wichtige Rolle in der Chemie. Zwei Enantiomere eines chiralen Moleküls können das polarisierte Licht in entgegengesetzte Richtungen drehen – eines nach links (levorotatorisch) und das andere nach rechts (dextrorotatorisch).
Die absolute Konfiguration eines Moleküls bestimmt seine spezifische optische Aktivität. Auch wenn zwei Enantiomere physikalisch gleich erscheinen können, haben sie doch sehr unterschiedliche Wirkungen auf polarisiertes Licht.
Der Enantiomerenüberschuss einer Mischung gibt an, wie stark eine Richtung der optischen Aktivität gegenüber der anderen vorherrscht. Dies ist besonders wichtig für Anwendungen wie die Pharmazie, wo oft nur ein Enantiomer therapeutisch nützlich ist. Chirale Trennungstechniken helfen dabei, diese spezifische Form des Moleküls abzutrennen.
Anwendungen in der Pharmazie und Medizin
Chiralität und Enantiomerie spielen in der Pharmazie und Medizin eine äußerst wichtige Rolle. Händigkeit von Molekülen bedeutet, dass viele Medikamente in zwei verschiedenen spiegelbildlichen Formen existieren können. Diese Spiegelbildisomere, auch Enantiomere genannt, haben oft unterschiedliche biologische Wirkungen.
Ein Beispiel dafür ist Thalidomid, ein bekanntes Medikament, das in den 1950er Jahren zur Behandlung von Übelkeit eingesetzt wurde. Während das eine Enantiomer erwünschte therapeutische Effekte hatte, führte das andere zu schweren Missbildungen bei Neugeborenen. Dies verdeutlich die Wichtigkeit der chiralen Trennung und der enantioselektiven Synthese, um sicherzustellen, dass nur das gewünschte Enantiomer im Medikament vorhanden ist.
In der modernen Pharmazie gibt es zahlreiche Methoden zur Trennung von razemischen Gemischen. Durch Polarimetrie kann beispielsweise festgestellt werden, welcher Anteil eines Gemischs aus welchem Enantiomer besteht. Zudem wird oft auf spezielle chirale Katalysatoren zurückgegriffen, um gezielt eins der beiden Enantiomere zu erzeugen.
Die richtige Anwendung und Kontrolle von Chiralität in pharmazeutischen Substanzen reduzieren nicht nur Risiken, sondern erhöhen auch die Wirksamkeit der Medikamente. Dieses Wissen hat zu erheblichen Fortschritten in der Entwicklung von Arzneimitteln geführt und trägt maßgeblich zur sicheren medizinischen Versorgung bei.
| Parameter | Beschreibung | Beispiel |
|---|---|---|
| Chiralität | Vorhandensein eines asymmetrischen Kohlenstoffatoms | Chirales Zentrum in der Milchsäure |
| Optische Aktivität | Drehung der Ebene des polarisierten Lichts | Dextrorotatorische und levorotatorische Enantiomere |
| Trennmethoden | Techniken zur Separation von Enantiomeren | Kristallisation, Chromatographie |
Stereochemie und chirale Katalysatoren
Chirale Katalysatoren spielen eine zentrale Rolle in der Stereochemie, insbesondere bei der enantioselektiven Synthese. Diese Katalysatoren ermöglichen die gezielte Herstellung einer bestimmten Raumstruktur eines Moleküls, was für viele Anwendungen in der Pharmazie und Medizin von großer Bedeutung ist.
Die Optische Isomerie, auch bekannt als Spiegelbildisomerie, resultiert aus der Händigkeit von Molekülen. Hier kann ein chiraler Katalysator genutzt werden, um eine bevorzugte Konfiguration zu erzeugen, wodurch die Effektivität und Selektivität chemischer Reaktionen verbessert wird. Dadurch wird sichergestellt, dass das gewünschte Enantiomer mit einem höheren Enantiomerenüberschuss gewonnen wird.
Ein Beispiel für den Einsatz solcher Katalysatoren findet man in der Synthese von Arzneimitteln. Hier können geringfügige Unterschiede in der Absolute Konfiguration eines Wirkstoffs erhebliche Auswirkungen auf dessen medizinische Wirkung oder Nebenwirkungen haben. Chirale Katalysatoren tragen dazu bei, diese Feinheiten zu kontrollieren und damit die Effizienz und Sicherheit von Arzneimitteln zu steigern.
Zusätzlich zur Pharmaindustrie sind chirale Katalysatoren auch in der Herstellung von Agrochemikalien und Spezialmaterialien wertvoll. Die Fähigkeit dieser Katalysatoren, bestimmte Enantiomere selektiv zu synthetisieren, ermöglicht es, maßgeschneiderte Verbindungen mit spezifischen physikalischen und chemischen Eigenschaften herzustellen.
Schließlich spielt die Entwicklung neuartiger chiraler Katalysatoren eine Schlüsselrolle bei der Weiterentwicklung moderner Stereochemie und der enantioselektiven Synthesetechniken, wobei stets ein Fokus auf Nachhaltigkeit und Umweltverträglichkeit gelegt wird.
Physikalische und chemische Eigenschaften vergleichen
Ein wichtiger Aspekt in der Chemie ist der Vergleich der physikalischen und chemischen Eigenschaften von Enantiomeren. Diese spiegelbildlichen Isomere besitzen identische physikalische Eigenschaften wie Schmelzpunkt, Siedepunkt und Dichte. Dennoch zeigen sie Unterschiede in ihrer Reaktivität gegenüber anderen chiralen Verbindungen.
Die meisten einzigartigen Eigenschaften von Enantiomeren entstehen aus ihrer Interaktion mit polarisiertem Licht und anderen chiralen Substanzen. So kann beispielsweise ein Enantiomer eine Drehung des polarisierten Lichts nach links bewirken, während das Spiegelbildisomer das Licht in die entgegengesetzte Richtung dreht.
Eine weitere bemerkenswerte Eigenschaft ist der Enantiomerenüberschuss. Dies bezieht sich auf das Vorhandensein eines Enantiomers in höherer Konzentration als das andere in eenem Mische enthaltene ist. Ein hoher Enantiomerenüberschuss kann bestimmte biologische Aktivitäten intensivieren oder abschwächen.
Auch in chemischer Hinsicht können sich Enantiomere unterschiedlich verhalten. Zum Beispiel kann ein Enantiomer eines Arzneimittels therapeutisch wirksam sein, während das andere unwirksam oder sogar toxisch sein könnte. Hier spielt die absolute Konfiguration eine entscheidende Rolle, da sie die spezifische räumliche Anordnung der Atome im Molekül definiert.
Der Vergleich dieser Eigenschaften ist daher unerlässlich in Bereichen wie Pharmazeutika und Biochemie, um die angemessene Nutzung und Effizienz von chiralen Verbindungen zu gewährleisten.
Synthese und Analyse chiraler Verbindungen
Die Synthese und Analyse chiraler Verbindungen sind zentrale Themen in der chemischen Forschung. Hierbei handelt es sich um Verfahren zur Herstellung und Untersuchung von Molekülen mit asymmetrischer Struktur, die nicht deckungsgleiche Spiegelbilder – sogenannte Enantiomere – hervorbringen.
Für die Synthese dieser Verbindungen gibt es verschiedene Methoden. Eine wichtige Methode ist die enantioselektive Synthese, bei der nur eines von zwei möglichen Enantiomeren bevorzugt gebildet wird. Dies kann durch den Einsatz von chiralen Katalysatoren oder Ausgangsstoffen erreicht werden, die eine gezielte Steuerung der Reaktion ermöglichen.
Nach der Synthese müssen die chiralen Verbindungen genau analysiert werden, um ihre Reinheit und Zusammensetzung zu bestimmen. Ein gängiges Verfahren hierzu ist die Polarimetrie. Mit diesem instrumentellen Ansatz lässt sich die optische Drehung einer Substanz messen, die direkt mit ihrer chiralen Reinheit zusammenhängt. Auch hochauflösende chromatographische Techniken wie HPLC (High Performance Liquid Chromatography) spielen eine entscheidende Rolle bei der Trennung und Quantifizierung von Enantiomeren.
Weiterhin kann mittels NMR-Spektroskopie (Kernspinresonanzspektroskopie) die molekulare Struktur untersucht werden, was Aufschluss über die absolute Konfiguration der chiralen Zentren geben kann. Insgesamt tragen diese methodischen Ansätze dazu bei, eine detaillierte Charakterisierung von chiralen Verbindungen zu ermöglichen, was für deren Anwendung in Bereichen wie Pharmazie und Medizin unerlässlich ist.