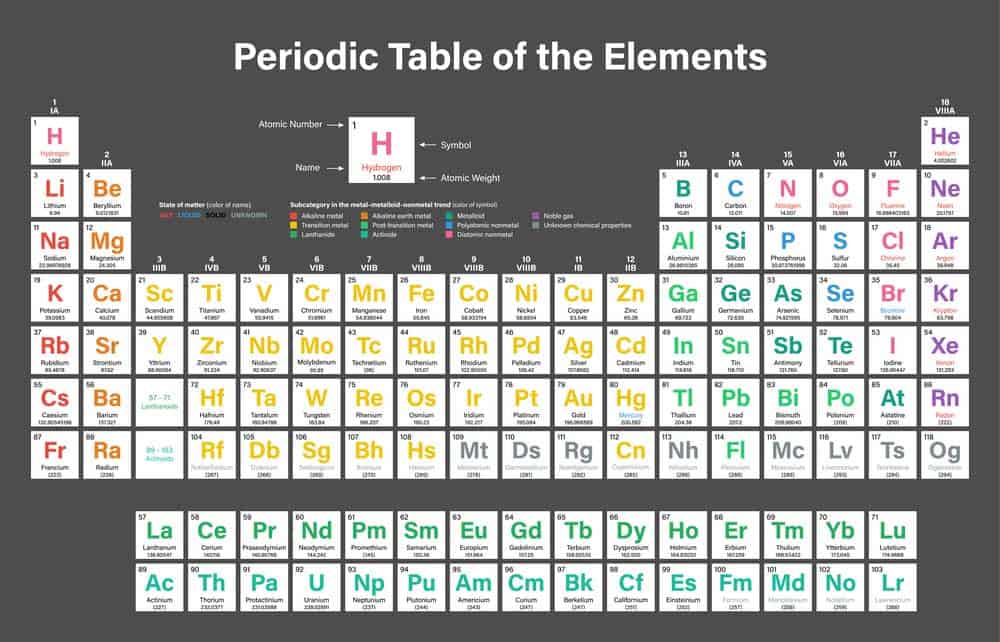
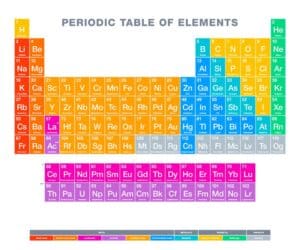
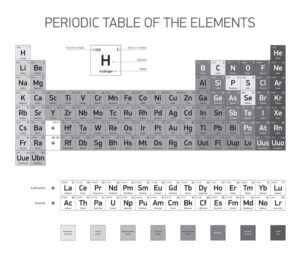
Das Periodensystem der Elemente ist ein zentrales Werkzeug in der Chemie, das die verschiedenen chemischen Elemente in einer bestimmten Ordnung auflistet. Innerhalb dieses Systems gibt es eine besondere Gruppe von Elementen: die Nebengruppen. Insgesamt umfasst das Periodensystem 10 Nebengruppen, die hauptsächlich aus den sogenannten Übergangsmetallen bestehen. Diese Metalle besitzen vielfältige chemische Eigenschaften und spielen eine wichtige Rolle in vielen technologischen und industriellen Anwendungen. Die erste Nebengruppe reicht von Scandium bis Zink, während die zweite Nebengruppe von Yttrium bis Cadmium reicht. Auch die Lanthanoide und Actinoide zählen zu diesen Nebengruppen und erweitern dadurch das Spektrum der Übergangsmetalle.
Das Wichtigste in Kürze
- Das Periodensystem umfasst 10 Nebengruppen, hauptsächlich Übergangsmetalle.
- Erste Nebengruppe: Scandium bis Zink, chemisch vielseitig.
- Zweite Nebengruppe: Yttrium bis Cadmium, breites Anwendungsspektrum.
- Lanthanoide und Actinoide zählen zu den Nebengruppen.
- Nebengruppenelemente haben mehrere Oxidationsstufen und katalytische Fähigkeiten.
Periodensystem umfasst 10 Nebengruppen
Das Periodensystem umfasst 10 Nebengruppen. Diese Nebengruppen sind eine wichtige Klassifizierung, die vor allem die sogenannten Übergangsmetalle beinhaltet.
Die erste Nebengruppe reicht von Scandium bis Zink und ist bekannt für ihre vielseitigen chemischen Eigenschaften. Sie sind nicht nur in der Industrie von großer Bedeutung, sondern auch in biologischen Systemen; beispielsweise spielt Eisen eine Schlüsselrolle bei vielen biochemischen Reaktionen.
In der zweiten Nebengruppe finden wir Elemente wie Yttrium bis Cadmium. Auch diese Metalle zeigen eine breite Palette an Anwendungsmöglichkeiten und chemischem Verhalten. Eine interessante Tatsache ist, dass diese Elemente oft komplexe Verbindungen bilden und daher ausgiebig in der Katalyse verwendet werden.
Lanthanoide und Actinoide zählen ebenfalls zu den Nebengruppen. Obwohl sie unter speziellen Bedingungen betrachtet werden, haben sie dennoch aufregende Anwendungen in Bereichen wie Elektronik, Medizin und Energieerzeugung. Häufig sieht man diese Elemente auch als seltene Erden betitelt.
Durch die Vielzahl ihrer chemischen Eigenschaften, wie unterschiedliche Oxidationsstufen und magnetische Charakteristika, bieten die Nebengruppen viele spannende Aspekte für das Studium und die praktische Anwendung.
Die Elemente der Nebengruppen sind das Herzstück der modernen Chemie und bieten unzählige Möglichkeiten für wissenschaftliche Innovation. – Robert H. Grubbs
| Nebengruppe | Elemente |
|---|---|
| Erste Nebengruppe | Scandium (Sc) bis Zink (Zn) |
| Zweite Nebengruppe | Yttrium (Y) bis Cadmium (Cd) |
| Lanthanoide | 58 Cer (Ce) bis 71 Lutetium (Lu) |
| Actinoide | 90 Thorium (Th) bis 103 Lawrencium (Lr) |
Nebengruppen umfassen Übergangsmetalle
Die Nebengruppen umfassen eine besondere Klasse von Elementen, die als Übergangsmetalle bekannt sind. Diese Elemente zeichnen sich durch ihre vielfältigen chemischen Eigenschaften aus und nehmen im Periodensystem eine zentrale Position ein.
Übergangsmetalle finden sich in den Gruppen 3 bis 12 des Periodensystems und spielen eine wesentliche Rolle in der Chemie. Sie haben teilweise gefüllte d-Orbitale, was ihnen einzigartige Eigenschaften verleiht, wie etwa färbige Komplexe zu bilden oder variable Oxidationsstufen einzunehmen.
Zu den bekannten Übergangsmetallen gehören Eisen, Kupfer und Nickel. Ihre Vielseitigkeit macht sie zu wichtigen Akteuren in vielen industriellen Prozessen. Beispielsweise ist Eisen ein Hauptbestandteil von Stahl, während Kupfer aufgrund seiner hervorragenden Leitfähigkeit weit verbreitet in elektrischen Kabeln genutzt wird.
Ein bemerkenswertes Merkmal der Übergangsmetalle ist ihre Fähigkeit, stabile Komplexverbindungen mit anderen Molekülen zu bilden. Dies liegt an den freien d-Orbitalen, die Elektronenpaare aufnehmen können, was zu der Bildung einer Vielzahl von chemischen Verbindungen führt.
Darüber hinaus zeigen diese Metalle häufig magnetische Eigenschaften. Ein Beispiel dafür ist Nickel, das in zahlreichen Anwendungen wie Magneten und Legierungen eingesetzt wird.
| Nebengruppe | Erste Elemente | Letzte Elemente |
|---|---|---|
| Erste Nebengruppe | Scandium (Sc) | Zink (Zn) |
| Zweite Nebengruppe | Yttrium (Y) | Cadmium (Cd) |
| Lanthanoide | 58 Cer (Ce) | 71 Lutetium (Lu) |
| Actinoide | 90 Thorium (Th) | 103 Lawrencium (Lr) |
Scandium bis Zink bilden erste Nebengruppe
Im Periodensystem befinden sich die Elemente von Scandium bis Zink in der sogenannten ersten Nebengruppe. Diese Gruppe bildet den Anfang der Übergangsmetalle, welche für ihre Vielseitigkeit und besonderen chemischen Eigenschaften bekannt sind.
Die Übergangsmetalle zeichnen sich durch teilweise gefüllte d-Orbitale aus, was zu ihrer besonderen Reaktivität führt. Innerhalb der ersten Nebengruppe findet man Elemente wie Vanadium, Chrom und Mangan, die jeweils einzigartige Anwendungen haben, zum Beispiel in Legierungen oder als Katalysatoren.
Ein wesentlicher Aspekt dieser Met alle ist ihre Fähigkeit, verschiedene Oxidationszustände einnehmen zu können. Dies ermöglicht eine breitere Palette an chemischen Reaktionen im Vergleich zu anderen Elementen. Zudem haben viele dieser Metalle eine hohe elektrische Leitfähigkeit und werden deshalb in der Elektrotechnik genutzt.
Mit den weiteren Mitgliedern wie Eisen, Cobalt und Nickel deckt die erste Nebengruppe fast sämtliche Bedarf am industriellen Einsatz ab. Zum Abschluss stößt man auf die Elemente Kupfer und Zink, die ebenfalls vielfältige industrielle Bedeutung besitzen.
Yttrium bis Cadmium in zweiter Nebengruppe
Die Elemente von Yttrium bis Cadmium befinden sich in der zweiten Nebengruppe des Periodensystems. Diese Gruppe ist bekannt für ihre einzigartigen chemischen Eigenschaften, die durch den Aufbau ihrer Elektronenhüllen bestimmt werden.
Nebengruppenelemente sind oftmals metaphorische Brücken zwischen anderen Elementgruppen und spielen eine entscheidende Rolle in vielen technologischen Anwendungen. Besonders wichtig ist dabei die Gruppe der Übergangsmetalle, zu denen auch Yttrium und Cadmium gehören.
Yttrium, beispielsweise, wird häufig in Hochleistungsmagneten genutzt und hat weitreichende Anwendungsmöglichkeiten insbesondere in der Elektronik und in der Medizin. Seine Fähigkeit, bei hohen Temperaturen stabil zu bleiben, macht es äußerst wertvoll.
Auf der anderen Seite steht Cadmium, das ebenfalls vielseitig verwendbar ist. Eine bedeutende Anwendung findet Cadmium in Nickel-Cadmium-Akkumulatoren, wo es aufgrund seiner elektrochemischen Stabilität geschätzt wird. Allerdings muss der Umgang mit Cadmium sorgfältig geregelt werden, da dieses Metall potenziell toxisch ist.
Mit ihren vielfältigen Eigenschaften und Funktionen tragen diese Übergangselemente wesentlich zur modernen Wissenschaft und Technik bei. Ihre chemische Vielseitigkeit und praktischen Anwendungen machen sie unverzichtbare Bestandteile vieler Schlüsseltechnologien.
Lanthanoide und Actinoide zählen zu den Nebengruppen
Die Lanthanoide und Actinoide zählen zu den Nebengruppen des Periodensystems. Diese beiden Serien, auch als seltene Erden und Actiniden bekannt, bestehen aus insgesamt 30 Elementen, die sich jeweils durch ihre einzigartigen chemischen Eigenschaften auszeichnen.
Lanthanoide sind Elemente mit den Ordnungszahlen 57 bis 71 und beinhalten bekannte Metalle wie Cer, Neodym und Europium. Sie werden oft in modernen Technologien eingesetzt, zum Beispiel in Permanentmagneten und Leuchtstoffen.
Actinoide, mit den Ordnungszahlen 89 bis 103, umfassen radioaktive Elemente wie Uran und Plutonium. Diese finden Anwendung in der Kernenergie und Nuklearmedizin.
Sowohl Lanthanoide als auch Actinoide verhalten sich ähnlich zu anderen Übergangsmetallen und weisen eine Vielzahl von Oxidationszuständen auf. Dies macht sie vielseitig einsetzbar und wertvoll für Industrie und Wissenschaft. Die elektronischen Konfigurationen dieser Elemente tragen wesentlich zu ihren spezifischen chemischen Reaktionen bei.
Obwohl sie traditionell unter den Hauptgruppenelementen gedacht wurden, erlaubt ihre Einordnung in die Nebengruppe eine übersichtlichere Darstellung im Periodensystem.
Nebengruppen haben vielseitige chemische Eigenschaften
Die Nebengruppen im Periodensystem zeichnen sich durch ihre vielseitigen chemischen Eigenschaften aus. Diese Elemente, die hauptsächlich Übergangsmetalle umfassen, haben oft mehrere Oxidationsstufen und können komplexe Verbindungen bilden.
Ein markantes Merkmal der Nebengruppenelemente ist ihre Fähigkeit zur Katalyse, da viele von ihnen als Katalysatoren in industriellen Prozessen verwendet werden. Zum Beispiel wird Platin häufig in der Fahrzeugkatalyse eingesetzt, um schädliche Abgase in weniger schädliche Stoffe umzuwandeln.
Darüber hinaus haben diese Metalle besondere physikalische Eigenschaften wie Magnetismus und Leitfähigkeit. Eisen, Kobalt und Nickel sind beispielsweise ferromagnetisch, was bedeutet, dass sie starke magnetische Felder erzeugen können.
Nebengruppenelemente wie Kupfer, Silber und Gold sind ausgezeichnete elektrische Leiter und finden breite Anwendung in der Elektronik- und Elektroindustrie. Ihre Vielseitigkeit spiegelt sich auch in der Verwendung in Legierungen wider; Bronze (eine Kupfer-Zinn-Legierung) und Messing (eine Kupfer-Zink-Legierung) sind typische Beispiele.
Diese Eigenschaften machen die Nebengruppenelemente zu unverzichtbaren Bestandteilen zahlreicher technischer und industrieller Anwendungen. Ob in der Herstellung von Stahl, elektronischen Bauteilen oder chemischen Katalysatoren – die Vielseitigkeit dieser Elemente spielt eine zentrale Rolle in verschiedenen Branchen.