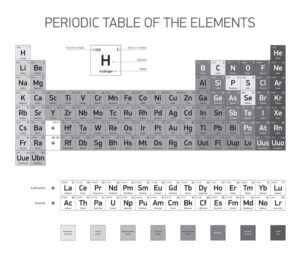
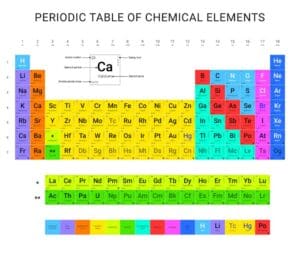
Das Periodensystem ist ein fundamentales Werkzeug der Chemie, das die Anordnung der chemischen Elemente veranschaulicht. In diesem System nehmen Metalle einen bedeutenden Platz ein. Alkalimetalle, Erdalkalimetalle und Übergangsmetalle sind Beispiele für verschiedene Metallklassen, die jeweils bestimmte Positionen im Periodensystem innehaben.
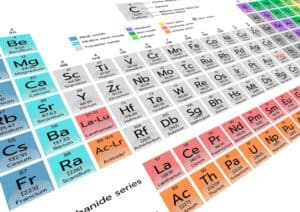
Die Metalle befinden sich überwiegend auf der linken Seite und in der Mitte des Periodensystems. Weiter unten findet man spezielle Serien wie die Lanthanoide und Actinoide. Es ist interessant zu beobachten, wie die verschiedenen Gruppen und Blöcke organisiert sind.
So erleichtert das Periodensystem das Verständnis für die physikalischen und chemischen Eigenschaften dieser Elemente.
Das Wichtigste in Kürze
- Metalle sind überwiegend auf der linken und mittleren Seite des Periodensystems angeordnet.
- Alkalimetalle und Erdalkalimetalle sind in den ersten beiden Gruppen des Periodensystems.
- Übergangsmetalle befinden sich in den mittleren Blöcken, Gruppen 3 bis 12.
- Lanthanoide und Actinoide sind am unteren Rand des Periodensystems dargestellt.
- Edelmetalle wie Gold und Silber sind korrosionsbeständig und wirtschaftlich wertvoll.
Metalle links und mittig im Periodensystem
Im Periodensystem der Elemente sind die Metalle überwiegend auf der linken Seite und in der Mitte zu finden. Diese Anordnung spiegelt ihre allgemeinen Eigenschaften wider, die sich deutlich von denen der Nichtmetalle unterscheiden.
In den ersten beiden Gruppen des Periodensystems befinden sich die Alkalimetalle und Erdalkalimetalle. Sie zeichnen sich durch ihre Reaktivität aus, wobei die Alkalimetalle besonders reaktionsfreudig sind. Dabei nehmen sie typischerweise Elektronen ab und bilden positiv geladene Ionen.
In der Mitte des Periodensystems sind die Übergangsmetalle angesiedelt. Dazu gehören bekannte Elemente wie Eisen, Kupfer und Nickel. Diese Metalle haben teilweise gefüllte d-Orbitale, was ihnen besondere chemische Eigenschaften verleiht und sie vielseitig einsetzbar macht. Übergangsmetalle spielen eine wichtige Rolle in verschiedenen industriellen Prozessen und Anwendungen, darunter als Katalysatoren in chemischen Reaktionen.
Die Lanthanoide und Actinoide finden sich hingegen am unteren Rand des Periodensystems, meist getrennt dargestellt, um die Tabelle übersichtlicher zu gestalten. Diese Elemente werden oft zur Herstellung von Hochtechnologieprodukten verwendet und besitzen einzigartige magnetische und elektronische Eigenschaften.
Durch diese klare Aufteilung im Periodensystem wird sofort ersichtlich, dass Metalle eine zentrale und vielfältige Gruppe innerhalb der Elemente darstellen.
Metalle sind die Seele der materiellen Welt, sie geben uns Struktur und Stabilität. – Marie Curie
| Metallklasse | Beispiel-Elemente |
|---|---|
| Alkalimetalle | Lithium (Li), Natrium (Na), Kalium (K) |
| Erdalkalimetalle | Magnesium (Mg), Calcium (Ca), Strontium (Sr) |
| Übergangsmetalle | Eisen (Fe), Kupfer (Cu), Nickel (Ni) |
| Lanthanoide | Lanthan (La), Cer (Ce), Neodym (Nd) |
| Actinoide | Uran (U), Plutonium (Pu), Thorium (Th) |
Alkalimetalle in der ersten Gruppe
In der ersten Gruppe des Periodensystems befinden sich die Alkalimetalle. Diese Gruppe umfasst Elemente wie Lithium (Li), Natrium (Na), Kalium (K), Rubidium (Rb), Cäsium (Cs) und Francium (Fr).
Alkalimetalle sind für ihre hohe Reaktivität bekannt. Sie reagieren sehr leicht mit Wasser und müssen daher in spezialisierten Behältern aufbewahrt werden, um eine unkontrollierte Reaktion zu verhindern.
Die chemischen Eigenschaften dieser Metalle resultieren aus ihrer Fähigkeit, ein einziges Elektron von ihrer äußersten Schale abzugeben, was sie stabiler macht. Dies führt dazu, dass sie besonders energisch mit anderen Elementen interagieren.
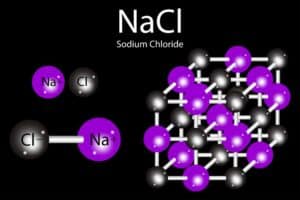
Ein weiterer interessanter Aspekt ist ihr Auftreten in Naturstoffen. Zum Beispiel kommt Natrium häufig in Form von Kochsalz (Natriumchlorid) vor und spielt eine wichtige Rolle im menschlichen Körper, insbesondere beim Nervensystem und der Muskelkontraktion.
Zusammengefasst zeichnen sich Alkalimetalle durch ihre außergewöhnlich hohe Reaktivität und ihre Rolle in verschiedenen natürlichen und industriellen Prozessen aus.
| Metallklasse | Gruppe im Periodensystem | Wichtige Nutzung |
|---|---|---|
| Alkalimetalle | 1 | Batterien, Wärmeübertragung |
| Erdalkalimetalle | 2 | Bauindustrie, medizinische Anwendungen |
| Übergangsmetalle | 3-12 | Bauwerke, Elektronik, Katalysatoren |
| Lanthanoide | 57-71 | Magnetische Materialien, optische Geräte |
| Actinoide | 89-103 | Kernenergie, medizinische Diagnostik |
Erdalkalimetalle in der zweiten Gruppe
Die Erdalkalimetalle befinden sich in der zweiten Gruppe des Periodensystems und umfassen die Elemente Beryllium, Magnesium, Calcium, Strontium, Barium und Radium. Diese Metalle zeichnen sich durch ihre hohe Reaktivität aus, obwohl sie weniger reaktiv sind als die Alkalimetalle der ersten Gruppe.
In chemischen Reaktionen neigen Erdalkalimetalle dazu, Elektronen abzugeben und bilden dadurch zweiwertige positive Ionen, bekannt als Kationen. Dadurch werden sie zu starken Reduktionsmitteln. Ein charakteristisches Merkmal dieser Elemente ist ihre Fähigkeit zur Bildung von stabilen Oxiden und Hydroxiden, die häufig eine wichtige Rolle in industriellen Anwendungen spielen.
Magnesium und Calcium sind vermutlich die bekanntesten Vertreter dieser Gruppe und haben bedeutende industrielle und biologische Anwendungen. Magnesium wird unter anderem in der Luft- und Raumfahrt sowie in der Fotoindustrie verwendet, während Calcium essenziell für den Aufbau von Knochen und Zähnen ist.
Diese Metalle präsentieren sich in ihrer natürlichen Form oft als Bestandteile von Mineralien und Gesteinen. Beispielsweise ist Kalkstein, der hauptsächlich aus Calciumcarbonat besteht, ein weit verbreitetes Gestein mit vielfältigen Verwendungen im Bauwesen.
Die chemischen Eigenschaften der Erdalkalimetalle machen sie zu einem interessanten Forschungsgebiet, insbesondere wegen ihrer vielfältigen Anwendungsmöglichkeiten.
Übergangsmetalle in den mittleren Blöcken
Übergangsmetalle befinden sich im Periodensystem der Elemente in den mittleren Blöcken, genauer gesagt in den Gruppen 3 bis 12. Diese Metalle zeichnen sich durch ihre umfangreichen chemischen Eigenschaften aus und spielen eine entscheidende Rolle in vielen industriellen Prozessen.
Ein zentrales Merkmal der Übergangsmetalle ist die Präsenz von d-Elektronen in ihren Atomen, was ihnen außergewöhnliche Katalysatoreigenschaften verleiht. Dadurch sind sie unverzichtbar für zahlreiche chemische Reaktionen, einschließlich der Herstellung von Kunststoffen, Medikamenten und Düngemitteln. Nicht nur in der Chemie, sondern auch in der Physik haben die Übergangsmetalle aufgrund ihrer besonderen elektrischen und magnetischen Eigenschaften immense Bedeutung.
Viele dieser Metalle wie Eisen, Kupfer und Nickel werden zudem wegen ihrer hervorragenden Leitfähigkeit und Widerstandsfähigkeit in der Elektronikindustrie hochgeschätzt. Ihre Legierungsfähigkeiten ermöglichen die Entwicklung von Werkstoffen mit spezifisch gewünschten Eigenschaften.
Die Übergangsmetalle unterscheiden sich stark in Bezug auf Härte, Schmelzpunkt und andere physikalische Eigenschaften. Dies ermöglicht es, sie in einer breiten Palette von Anwendungen einzusetzen, von Münzen über Bauwerke bis hin zu fortschrittlichen technischen Geräten.
Zusammen ergeben diese Faktoren ein klares Bild von der zentralen Position der Übergangsmetalle innerhalb des Periodensystems und ihrer umfangreichen Nützlichkeit in zahlreichen modernen Technologien.
Lanthanoide und Actinoide unten angeordnet
Die Lanthanoide und Actinoide finden sich im Periodensystem in einer separaten Anordnung am unteren Rand. Diese Metalle werden häufig als seltene Erden bezeichnet, obwohl einige von ihnen gar nicht so selten sind. In der Realität sind sie wegen ihrer chemischen Eigenschaften schwerer zu trennen.
Lanthanoide umfassen die Elemente mit den Ordnungszahlen 57 bis 71. Sie haben ähnliche chemische Eigenschaften und kommen oft zusammen in natürlichen Mineralien vor. Bekannt sind sie unter anderem für ihre Verwendung in leistungsstarken Magneten und Leuchtstoffen.
Actinoide, auf der anderen Seite, umfassen die Elemente mit den Ordnungszahlen 89 bis 103. Viele dieser Metalle, insbesondere Uran und Plutonium, spielen eine Schlüsselrolle in kerntechnischen Anwendungen.
Aufgrund ihrer speziellen elektronischen Konfiguration unterscheiden sie sich klar von den übrigen Elementen. Ihre Platzierung in zwei eigenen Reihen erleichtert das Lesen des Periodensystems erheblich und sorgt zugleich für eine übersichtliche Struktur.
Edelmetalle in der elften Gruppe
Die Edelmetalle befinden sich im Periodensystem in der elften Gruppe. Diese Metalle sind für ihre besonderen Eigenschaften bekannt, die sie von vielen anderen Elementen unterscheiden.
Zu den wichtigsten Edelmetallen gehören Gold (Au), Silber (Ag) und Kupfer (Cu). Sie zeichnen sich durch ihre außerordentliche Korrosionsbeständigkeit aus, was bedeutet, dass sie nicht leicht oxidieren oder rosten.
Edelmetalle werden häufig in Schmuck, elektronischen Bauteilen und Münzen verwendet. Ihre hervorragende elektrische Leitfähigkeit macht sie auch in der Elektronikindustrie unverzichtbar.
Ein weiteres Merkmal der Edelmetalle ist ihr hoher wirtschaftlicher Wert. Gold und Silber zum Beispiel haben eine lange Geschichte als Zahlungsmittel und Investitionsobjekte.
Neben ihren praktischen Anwendungen spielen Edelmetalle auch eine wichtige Rolle in verschiedenen wissenschaftlichen Bereichen, etwa in der Katalyse oder in medizinischen Geräten. Trotz ihrer Seltenheit und dem oft hohen Preis bleiben Edelmetalle aufgrund ihrer einzigartigen Eigenschaften unersetzlich.
So zeigt sich deutlich, dass die Edelmetalle der elften Gruppe des Periodensystems einen wesentlichen Beitrag sowohl in technologischer als auch in wirtschaftlicher Hinsicht leisten können.