Die chemischen Elemente sind die fundamentalen Bausteine unserer materiellen Welt. Eine offizielle Liste der Elemente beinhaltet derzeit 118 bekannte Elemente, welche in einer alphabetischen Anordnung präsentiert werden können. Diese alphabetische Ordnung ist besonders hilfreich für diejenigen, die spezifische Informationen schnell finden möchten.
Das Periodensystem spielt eine zentrale Rolle bei der Klassifizierung und Organisation dieser Elemente. Es bietet eine Übersicht über wichtige Details wie Atomzahl, Symbol und Masse. Die Nomenklatur der Chemie ist dabei ein wesentliches Instrument: Sie gewährleistet Klarheit und Konsistenz bei der Benennung und Identifikation von Elementen.
Im Alltag begegnen uns viele dieser Elemente in verschiedensten Formen und Anwendungen – vom Aluminium in Getränkedosen bis zum Sauerstoff, den wir atmen. Historisch betrachtet haben zahlreiche Entdeckungen dieser Elemente maßgeblich zur Entwicklung unserer heutigen Wissenschaft und Technologie beigetragen. Eine elementarische Tabelle ermöglicht es, diese Fülle an Informationen strukturiert darzustellen.
Das Wichtigste in Kürze
- 118 bekannte chemische Elemente, geordnet im Periodensystem nach Atomen und Eigenschaften.
- Periodensystem zeigt Ordnungszahl, Symbol und atomare Masse der Elemente.
- Vielseitige Anwendungen von Metallen, Sauerstoff und Kohlenstoff im Alltag.
- Elemente wurden durch historische Entdeckungen und moderne Techniken identifiziert.
- Nomenklatur und alphabetische Anordnung erleichtert das Lernen und Forschen.
| Element | Abkürzung |
|---|---|
| Actinium | Ac |
| Aluminium | Al |
| Americium | Am |
| Antimon | Sb |
| Argon | Ar |
| Barium | Ba |
| Beryllium | Be |
| Bismut | Bi |
| Bohrium | Bh |
| Bor | B |
| Brom | Br |
| Cadmium | Cd |
| Calcium | Ca |
| Californium | Cf |
| Cer | Ce |
| Cäsium | Cs |
| Chlor | Cl |
| Chrom | Cr |
| Cobalt | Co |
| Curium | Cm |
| Darmstadtium | Ds |
| Dubnium | Db |
| Dysprosium | Dy |
| Einsteinium | Es |
| Erbium | Er |
| Europium | Eu |
| Eisen | Fe |
| Fermium | Fm |
| Flerovium | Fl |
| Fluor | F |
| Francium | Fr |
| Gadolinium | Gd |
| Gallium | Ga |
| Germanium | Ge |
| Gold | Au |
| Hafnium | Hf |
| Hassium | Hs |
| Helium | He |
| Holmium | Ho |
| Indium | In |
| Iod | I |
| Jod | I |
| Kalium | K |
| Kadmium | Cd |
| Kupfer | Cu |
| Lanthan | La |
| Lawrencium | Lr |
| Lithium | Li |
| Livermorium | Lv |
| Lutetium | Lu |
| Magnesium | Mg |
| Mangan | Mn |
| Meitnerium | Mt |
| Molybdän | Mo |
| Natrium | Na |
| Neodym | Nd |
| Neon | Ne |
| Nihonium | Nh |
| Niob | Nb |
| Nickel | Ni |
| Nihonium | Nh |
| Natrium | Na |
| Neodym | Nd |
| Nobelium | No |
| Osmium | Os |
| Phosphor | P |
| Palladium | Pd |
| Platin | Pt |
| Polonium | Po |
| Praseodym | Pr |
| Protactinium | Pa |
| Radium | Ra |
| Radon | Rn |
| Rhenium | Re |
| Rhodium | Rh |
| Rubidium | Rb |
| Ruthenium | Ru |
| Rutherfordium | Rf |
| Sauerstoff | O |
| Samarium | Sm |
| Scandium | Sc |
| Schwefel | S |
| Seaborgium | Sg |
| Selen | Se |
| Silber | Ag |
| Stickstoff | N |
| Strontium | Sr |
| Tantal | Ta |
| Technetium | Tc |
| Tellur | Te |
| Tennessin | Ts |
| Terbium | Tb |
| Thallium | Tl |
| Thorium | Th |
| Thulium | Tm |
| Titan | Ti |
| Tungsten | W |
| Uran | U |
| Vanadium | V |
| Wasserstoff | H |
| Wolfram | W |
| Xenon | Xe |
| Ytterbium | Yb |
| Yttrium | Y |
| Zink | Zn |
Einführung in chemische Elemente
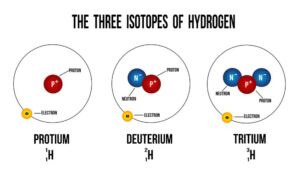
Chemische Elemente sind die grundlegenden Bestandteile aller Materie und eine zentrale Säule der Chemie. Jedes einzelne Element besteht aus Atomen, von denen jedes eine eindeutige Anzahl an Protonen im Atomkern aufweist. Diese Protonenzahl definiert das spezifische chemische Verhalten des Elements und erlaubt seine klare Identifizierung.
Die Bedeutung der Elemente wird oft durch das Periodensystem verdeutlicht, welches eine systematische Anordnung dieser Bausteine liefert. Das Periodensystem erlaubt nicht nur einen einfachen Zugriff auf entscheidende Informationen wie Ordnungszahl, Symbol und atomare Masse, sondern auch das Erkennen von Trends innerhalb bestimmter Gruppen und Perioden.
Im Alltag begegnen uns chemische Elemente ständig – sei es in Form von Sauerstoff, den wir atmen, oder Eisen, das in Konstruktionen verwendet wird. Die Namen von Elementen leiten sich oft von lateinischen oder griechischen Wörtern ab und spiegeln historische Entdeckungen oder Eigenschaften wider. Aufgrund ihrer Anschaulichkeit sind sie in zahlreichen Anwendungen überaus wertvoll und finden Verwendung in der Medizin, Technik sowie Umweltwissenschaften.
Die alphabetische Ordnung der Elemente erleichtert das Lernen der Elementnamen und deren Position im Periodensystem. Ob SchülerInnen, Studierende oder Fachleute – alle profitieren von einer klar strukturierten Liste der Elemente, welche die Einteilung und Nomenklatur der Chemie transparent macht und so den Chemikeralltag vereinfacht.
Ich glaube, dass die chemischen Elemente und ihre Verbindungen die Grundlage all unserer modernen technischen Fortschritte bilden. – Dmitri Mendelejew
Alphabetische Anordnung der Elemente
Das Periodensystem kann auf vielfältige Weise geordnet werden, jedoch hat sich die alphabetische Anordnung der Elemente als besonders hilfreich für den schnellen Überblick erwiesen. In dieser Liste sind die Namen der Elemente von A bis Z aufgeführt, was es einfach macht, spezifische Elemente zu finden.
Diese Methode berücksichtigt weder die chemischen Eigenschaften noch die Atomnummern, sondern stellt die Elementbezeichnungen lediglich in alphabetischer Reihenfolge dar. So kann man beispielsweise leicht feststellen, dass „Argon“ vor „Blei“ und „Sauerstoff“ nach „Stickstoff“ kommt.
Die Alphabetische Ordnung der Elementnamen ist nützlich bei der Verwendung verschiedener Referenzmaterialien wie Lehrbüchern oder wissenschaftlichen Artikeln. Es erlaubt eine schnelle Navigation und erleichtert das Auffinden von Informationen über ein bestimmtes Element.
In vielen Schulen und Universitäten wird diese Methode genutzt, um den Lernenden die Nomenklatur Chemie näherzubringen. Listen wie diese sind auch oft im Internet verfügbar und dienen als praktische Werkzeuge für alle, die einen schnellen Zugang zu präzisen Daten benötigen.
Durch die Verwendung einer alphabetischen Liste der Elemente können Wissenschaftler, Lehrer, Studenten und Laien gleichermaßen effizient arbeiten und recherchieren. Diese Form der Anordnung bietet eine klare und einfache Möglichkeit, die Fülle an Wissen über chemische Elemente zu strukturieren und zugänglich zu machen.
| Elementname | Symbol |
|---|---|
| Wasserstoff | H |
| Helium | He |
| Kohlenstoff | C |
| Sauerstoff | O |
| Stickstoff | N |
Anwendung chemischer Elemente im Alltag
Chemische Elemente spielen eine entscheidende Rolle in unserem alltäglichen Leben und finden sich in zahlreichen Anwendungen wieder. Zum Beispiel ist Kohlenstoff (C) ein Schlüsselelement, das im menschlichen Körper als Teil von Proteinen, Fetten und Kohlenhydraten vorkommt.
Mehrere Metalle wie Eisen (Fe) und Aluminium (Al) sind nicht nur in der Elektronik und Bauindustrie weit verbreitet, sondern auch in Haushaltsgeräten und Fahrzeugen. Eisen wird hauptsächlich für die Herstellung von Stahl verwendet, während Aluminium aufgrund seiner Leichtigkeit in Luft- und Raumfahrtanwendungen beliebt ist.
Sauerstoff (O), ein weiteres bedeutendes Element, wird in medizinischen Anwendungen zur Unterstützung bei Atemproblemen eingesetzt und ist zudem unerlässlich für die Verbrennung in Motoren. Zusätzlich findet man Sauerstoff in Wasser, welches zentral für unser Überleben ist.
Seltene Erden, obwohl weniger bekannt, sind unverzichtbar in modernen Technologien wie Smartphones, Computern und Hybridfahrzeugen. Diese Elemente ermöglichen es, effizientere Batterien und leistungsfähigere Magnete herzustellen.
Weiterhin gibt es chemische Elemente wie Chlor (Cl), die in Reinigungsmitteln und Desinfektionsmitteln Anwendung finden, um Bakterien abzutöten und Hygiene zu gewährleisten. Somit verdeutlicht sich die immense Bedeutung chemischer Elemente in verschiedensten Lebensbereichen.
Diese Beispiele zeigen lediglich einen kleinen Ausschnitt der umfangreichen Verwendungszwecke chemischer Elemente auf und unterstreichen die grundlegende Relevanz dieser winzigen Bausteine unseres Universums.
Historische Entdeckung der Elemente
Die Entdeckung chemischer Elemente hat eine lange und faszinierende Geschichte. Bereits in der Antike unterschieden Alchemisten verschiedene Substanzen, ohne dass sie den heutigen Elementen vollständig entsprachen. Die moderne chemische Nomenklatur begann jedoch erst im 17. und 18. Jahrhundert.
Der schwedische Chemiker Carl Wilhelm Scheele und der englische Wissenschaftler Henry Cavendish machten bedeutende Entdeckungen. Sie isolierten zahlreiche Gase wie Sauerstoff und Wasserstoff. Im Jahr 1789 stellte Antoine Lavoisier die erste umfassende Liste bekannter Elemente auf, die als Vorläufer des modernen Periodensystems gilt.
Mit dem Fortschritt der analytischen Methoden konnten viele neue Elemente entdeckt werden. Dmitri Mendelejew entwickelte 1869 das erste Periodensystem, wobei er feststellte, dass sich die Eigenschaften der Elemente in regelmäßigen Abständen wiederholen. Dies half bei der Vorhersage der Existenz und Eigenschaften bislang unentdeckter Elemente.
Im 20. Jahrhundert erlaubten fortschrittliche Techniken wie Röntgenspektroskopie und Partikelbeschleuniger die Entdeckung zusätzlicher, oft sehr instabiler Elemente. Diese Entwicklungen wurden von internationalen Teams vorangetrieben, was zur Erweiterung des chemischen Katalogs führte.
Zusammenfassend veranschaulicht die geschichtliche Entwicklung der chemischen Elemente, inklusive ihrer Namen und Nomenklatur in der Chemie, nicht nur wissenschaftlichen Fortschritt, sondern auch die Bemühungen vieler talentierter Einzelpersonen und ihre Beiträge zu unserem Verständnis der Natur.
Übersicht chemischer Eigenschaftengruppen
Die chemischen Elemente sind in Gruppen eingeteilt, die nach ihren ähnlichen Eigenschaften klassifiziert sind. Diese Gruppierung hilft, das Verständnis für ihre Reaktivität, Verbindungen und Anwendungen zu erleichtern.
Eine der bekanntesten Eigenschaftengruppen sind die Alkalimetalle, die in der ersten Hauptgruppe des Periodensystems stehen. Diese Elemente wie Lithium und Natrium zeichnen sich durch ihre hohe Reaktionsfreudigkeit aus, insbesondere mit Wasser.
Ein weiterer wichtiger Abschnitt sind die Edelgase in der achten Hauptgruppe. Diese Gase wie Helium und Neon sind bekannt für ihre geringe Reaktivität und finden vielfach Anwendung, zum Beispiel in Beleuchtungssystemen.
Zu den Halogenen gehören Elemente wie Fluor und Chlor. Sie sind in der siebten Hauptgruppe zu finden und sind besonders reaktionsfreudig mit Metallen, wodurch Salze entstehen.
Die Erdalkalimetalle befinden sich in der zweiten Hauptgruppe und umfassen Elemente wie Magnesium und Calcium. Diese sind weniger reaktiv als die Alkalimetalle, spielen aber eine wichtige Rolle in biologischen Systemen und industriellen Anwendungen.
Durch diese Übersicht der chemischen Eigenschaftengruppen kann man grundlegende Konzepte und Klassifikationen besser verstehen, was auch die Handhabung von Elementen im Labor und in der Industrie vereinfacht.
Bedeutung chemischer Nomenklatur
Das Verständnis der Nomenklatur Chemie ist entscheidend für eine korrekte und präzise Kommunikation in der Wissenschaft. Nomenklatur bezieht sich auf das systematische Benennen von chemischen Verbindungen und Elementen. Die Elementbezeichnungen dienen nicht nur der klaren Identifikation, sondern auch der Klassifizierung und Organisation der Elemente innerhalb des Periodensystems.
Ein wesentlicher Aspekt bei der Benennung chemischer Elemente ist ihr lateinischer oder griechischer Ursprung. So leitet sich beispielsweise der Name „Natrium“ vom Lateinischen Wort „natrium“ ab, was in anderen Sprachen als „soda“ bekannt ist. Dies zeigt, wie die historische Herkunft eines Elementnamens zu seiner modernen Bezeichnung führt.
Auch die Unterscheidung zwischen ähnlichen Elementen wird durch die Nomenklatur vereinfacht. Zum Beispiel unterscheiden sich Eisen (Fe) und Fluor (F) nicht nur in ihren chemischen Eigenschaften, sondern auch in ihren spezifischen Abkürzungen und Namen, was Verwechslungen vermeidet. Solche Benennungen sind in einer umfassenden Liste der Elemente aufgeführt und erleichtern sowohl den wissenschaftlichen Austausch als auch das alltägliche Lernen und Lehren von chemischen Konzepten.
Zusammengefasst unterstützt die Nomenklatur die klare Zuordnung und einheitliche Beschreibung der ~Namen von Elementen~ und ihrer Verbindungen, was insbesondere im internationalen wissenschaftlichen Dialog von großer Bedeutung ist.
Struktur und Verwendung des Periodensystems
Das Periodensystem stellt eine geordnete und systematische Struktur chemischer Elemente dar. Die Elemente sind in Reihen, bekannt als Perioden, und Spalten, genannt Gruppen, angeordnet. Diese Anordnung basiert auf den Atomnummern der Elemente und deren chemischen Eigenschaften.
Die Verwendung des Periodensystems ist vielseitig. Es dient nicht nur zur Kategorisierung und Einteilung der Elemente, sondern auch als Werkzeug für Wissenschaftler, um Reaktionen vorherzusagen und neue Materialien zu entwickeln. Ingenieure, Chemiker und Physiker nutzen das Periodensystem täglich, um ihre Arbeit effizienter zu gestalten.
Ein wesentlicher Aspekt des Periodensystems ist seine Fähigkeit, die Wechselbeziehungen zwischen verschiedenen Elementen sichtbar zu machen. Beispielsweise zeigen Elemente innerhalb einer Gruppe ähnliche chemische und physikalische Eigenschaften. Dies ermöglicht es, Trends innerhalb derselben Spalte zu erkennen und vorherzusehen.
Darüber hinaus hilft das Periodensystem dabei, unbekannte oder weniger bekannte Elemente besser zu verstehen. Durch die genaue Positionierung kann man Rückschlüsse auf die Eigenschaften neuer bzw. seltener Elemente ziehen. Diese Methode erleichtert Forschern das Voranschreiten in vielen technologischen und wissenschaftlichen Disziplinen.
Elemente in Natur und Wissenschaft
Chemische Elemente spielen sowohl in der Natur als auch in der Wissenschaft eine zentrale Rolle. Sie sind die fundamentalen Bausteine, aus denen alle Materie besteht, und sie bestimmen wesentliche Eigenschaften von Substanzen.
In der Natur finden sich chemische Elemente in unterschiedlichen Formen: reine Elemente, Verbindungen und Gemischen. Ein Beispiel ist Kohlenstoff, das in Form von Diamanten, Graphit und organischen Molekülen vorkommt. Weiterhin sind viele industrielle Prozesse direkt abhängig von spezifischen Elementen wie Eisen für Stahlproduktion oder Silizium für elektronische Bauteile.
In der wissenschaftlichen Forschung ermöglichen chemische Elemente technologische Fortschritte und vertiefte Einblicke in die Struktur der Materie. Mithilfe des Periodensystems, das eine systematische Anordnung aller bekannten Elemente bietet, können Chemiker und Physiker Vorhersagen über deren chemische und physikalische Eigenschaften treffen. Diese geordnete Darstellung erleichtert das Auffinden von „Elementnamen“ und schafft eine Übersichtlichkeit, die für detaillierte Analysen notwendig ist.
Zusammenfassend bieten chemische Elemente einen unentbehrlichen Rahmen für unsere tägliche Existenz und den Ausbau technischen Wissens. Ihre alphabetische Gliederung und Nomenklatur helfen dabei, ihre komplexe Welt besser zu verstehen und gezielt anzuwenden.