Chemische Reaktionen mit Stoffbildung
Die Herstellung chemischer Stoffe durch gezielte Reaktionen hat einen hohen Stellenwert in der anorganischen Chemie sowie in den Naturwissenschaften generell. Ob es sich um das Haber-Bosch-Verfahren zur Herstellung von Ammoniak oder die Synthese von Aspirin handelt, diese Prozesse haben maßgeblich dazu beigetragen, viele Bedürfnisse unserer modernen Gesellschaft zu erfüllen. Die Fähigkeit, chemische Zusammensetzungen präzise zu kontrollieren und zu reproduzieren, ermöglicht eine kontinuierliche Versorgung mit wichtigen Substanzen.
Ein prominentes Beispiel ist die Verbindung von Wasserstoff und Sauerstoff zu H2O, welches als Hauptbestandteil von Flüssigkeiten im täglichen Leben agiert. Diese chemische Zusammensetzung zeigt eindrucksvoll, wie sich die Definition organisch und anorganisch voneinander unterscheiden kann. Wasser ist ein kohlenstofffreies Molekül und spielt doch eine zentrale Rolle in vielen chemischen Reaktionen mit Wasser. Durch ein tieferes Verständnis der Molekülstruktur und den Eigenschaften von Wasser wird das Feld der Chemie ständig erweitert.
Das Wichtigste in Kürze
- Das Haber-Bosch-Verfahren wandelt Stickstoff und Wasserstoff in Ammoniak für Düngemittelproduktion um.
- Schwefelsäure wird durch Kontaktverfahren aus Schwefeldioxid und Wasser mit Katalysatoren hergestellt.
- Ziegler-Natta-Katalysatoren ermöglichen die energieeffiziente Synthese von Polyethylen bei niedrigen Temperaturen.
- Fischer-Tropsch-Synthese konvertiert Kohlenmonoxid und Wasserstoff zu Methan und anderen Kohlenwasserstoffen.
- Die Chloralkali-Elektrolyse produziert Chlor, Wasserstoff und Natriumhydroxid aus gesättigter Salzlösung.
Eine chemische Reaktion, bei der ein Stoff gezielt hergestellt wird, ist eine Synthesereaktion. Bei einer Synthesereaktion reagieren zwei oder mehr Ausgangsstoffe miteinander, um einen gewünschten Stoff zu bilden. Diese Reaktion wird häufig durch gezielte Bedingungen wie Temperatur, Druck und Katalysatoren gesteuert, um den gewünschten Endstoff effizient zu produzieren.
| Chemische Reaktion | Produktherstellung |
|---|---|
| Haber-Bosch-Verfahren | Herstellung von Ammoniak |
| Kontaktverfahren | Herstellung von Schwefelsäure |
| Ziegler-Natta-Polymerisation | Synthese von Polyethylen |
| Fischer-Tropsch-Synthese | Herstellung von Methan |
| Acetylierung von Salicylsäure | Synthese von Aspirin |
| Chloralkali-Elektrolyse | Produktion von Chlor und Natriumhydroxid |
| Fermentation von Glukose | Herstellung von Ethanol |
| Polykondensation | Synthese von Nylon |
Synthesereaktion – genauer erklärt
Bei einer Synthesereaktion handelt es sich um eine chemische Reaktion, bei der zwei oder mehr Ausgangsstoffe miteinander reagieren, um einen neuen Stoff zu bilden. Diese Reaktion wird oft auch als Kondensationsreaktion bezeichnet. Das Ziel einer Synthesereaktion ist es, einen spezifischen Stoff gezielt herzustellen.
In der Regel wird bei einer Synthesereaktion eine oder mehrere chemische Bindungen zwischen den Ausgangsstoffen gebrochen, um neue Bindungen zu bilden. Dieser Vorgang erfordert Energie, die in Form von Wärme, Licht oder anderen Energiequellen zugeführt werden kann. Die Reaktionsbedingungen wie Temperatur, Druck und die Anwesenheit von Katalysatoren können beeinflussen, wie effizient die Synthesereaktion verläuft und welcher Endstoff gebildet wird.
Synthesereaktionen sind in vielen Bereichen der Chemie von großer Bedeutung, sei es in der organischen Chemie zur Herstellung von organischen Verbindungen oder in der anorganischen Chemie zur Synthese anorganischer Materialien. Die gezielte Herstellung von Stoffen durch Synthesereaktionen spielt eine wichtige Rolle in der Entwicklung neuer Materialien, Medikamente und vieler anderer Produkte, die in verschiedenen Industriezweigen verwendet werden.
Beispiele:
Diese folgenden chemischen Reaktionen stellen Stoffumwandlungen dar. In chemischen Reaktionen werden Ausgangsstoffe in neue Produkte umgewandelt, wobei die chemische Zusammensetzung der beteiligten Stoffe verändert wird. Dieser Prozess der Umwandlung von Ausgangsstoffen in Produkte wird als Stoffumwandlung bezeichnet.
- Die Synthese von Wasser: 2H₂ + O₂ → 2H₂O
- Herstellung von Salzsäure: HCl + H₂O → H₃O⁺ + Cl⁻
- Synthese von Ammoniak: N₂ + 3H₂ → 2NH₃
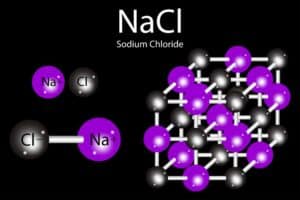
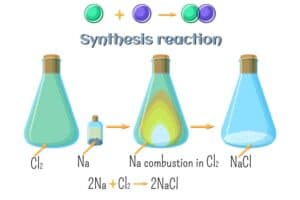
- Bildung von Natriumchlorid: 2Na + Cl₂ → 2NaCl
- Synthese von Schwefelsäure: SO₂ + O₂ + H₂O → H₂SO₄
- Herstellung von Ethanol: C₆H₁₂O₆ → 2C₂H₅OH + 2CO₂
- Synthese von Methan: C + 4H₂ → CH₄
- Bildung von Calciumoxid: 2Ca + O₂ → 2CaO
- Herstellung von Nylon: nH₂N-(CH₂)₆-NH₂ + nHOOC-(CH₂)₄-COOH → [HN-(CH₂)₆-NH-CO-(CH₂)₄-COO]ₙ + nH₂O
- Synthese von Glucose in der Photosynthese: 6CO₂ + 6H₂O + Lichtenergie → C₆H₁₂O₆ + 6O₂
- Herstellung von Siliziumdioxid: Si + O₂ → SiO₂
- Synthese von Polyethylen: nC₂H₄ → -(-CH₂-CH₂-)ₙ
Herstellung von Ammoniak durch Haber-Bosch-Verfahren
Das Haber-Bosch-Verfahren ist eine maßgebliche chemische Reaktion zur Herstellung von Ammoniak (NH3). Diese synthetische Methode kombiniert Stickstoff aus der Luft mit Wasserstoff, oft gewonnen aus Erdgas oder anderen Kohlenwasserstoffen. Hierbei handelt es sich um einen extrem wichtigen Prozess in den Naturwissenschaften und der Industrie, da Ammoniak ein Hauptbestandteil für die Produktion von Dünger ist.
Das Verfahren läuft unter hohem Druck und bei hohen Temperaturen ab, wobei eisenbasierte Katalysatoren verwendet werden, um die Reaktion zu beschleunigen. Die chemische Zusammensetzung von Ammoniak ermöglicht vielfältige Anwendungen, insbesondere in der Landwirtschaft, aber auch in der Herstellung von Kunststoffen und Sprengstoffen.
Ein besonders spannender Aspekt des Haber-Bosch-Verfahrens ist seine Bedeutung für die Chemie. Es demonstriert eindrucksvoll, wie durch gezielte Manipulation der Molekülstruktur und -zusammensetzung spezifische chemische Bindungen entstehen können. Hierdurch wird das im H2O Molekül enthaltene Wasserstoff in signifikanten Mengen verfügbar gemacht, obwohl es zuvor fest gebunden war.
Diese Reaktion zeigt auch die Verbindung von organischer und anorganischer Chemie, indem kohlenstofffreie Moleküle in einer Weise manipuliert werden, dass sie für menschliche Bedürfnisse nützlich sind. Der detaillierte Einblick in die chemischen Prozesse hinter dem Haber-Bosch-Verfahren bietet eine faszinierende Perspektive auf die Synthese und Nutzung chemischer Verbindungen.
Chemie kann man als die Kunst bezeichnen, Stoffe zu schaffen und zu verwandeln. – Justus von Liebig
Was ist das Haber-Bosch-Verfahren?
Das Haber-Bosch-Verfahren ist ein industrieller Prozess zur großtechnischen Herstellung von Ammoniak (NH₃) aus den Elementen Stickstoff (N₂) und Wasserstoff (H₂). Dieser Prozess wurde von Fritz Haber und Carl Bosch in den frühen 1900er Jahren entwickelt und ist eines der bedeutendsten Verfahren in der chemischen Industrie.
Im Haber-Bosch-Verfahren werden Stickstoff und Wasserstoff unter hohem Druck und hoher Temperatur in Gegenwart eines geeigneten Katalysators, wie z.B. Eisen-Katalysator, miteinander umgesetzt. Dabei entsteht Ammoniak als Hauptprodukt. Diese Reaktion ist exotherm, was bedeutet, dass sie Wärme freisetzt.
Die Herstellung von Ammoniak durch das Haber-Bosch-Verfahren ist von großer Bedeutung für die Düngemittelproduktion und ermöglicht eine effiziente Nutzung von Stickstoff aus der Luft zur Herstellung von Ammoniak. Ammoniak wird nicht nur als Düngemittel verwendet, sondern auch als Ausgangsstoff für die Herstellung von anderen Chemikalien wie Harnstoff, Nitrate und Kunststoffe.
Herstellung von Schwefelsäure durch Kontaktverfahren
Die Herstellung von Schwefelsäure durch das Kontaktverfahren ist ein zentraler Prozess in der chemischen Industrie. Bei dieser Methode wird Schwefeldioxid (chemische Zusammensetzung: SO2) katalytisch zu Schwefeltrioxid oxidiert, welches dann mit Wasser reagiert, um Schwefelsäure zu bilden.
Der Prozess beginnt mit der Verbrennung von Schwefel oder schwefelhaltigen Verbindungen, wobei Schwefeldioxid entsteht. Dieses Gas wird anschließend gereinigt und in einen Reaktor eingeleitet, wo es mittels eines vanadiumoxid-haltigen Katalysators zu Schwefeltrioxid oxidiert wird. Die Oxidationsreaktion läuft bei kontrollierter Temperatur (etwa 400-600°C) ab, um eine maximale Ausbeute an Schwefeltrioxid zu gewährleisten.
Das entstandene Schwefeltrioxid wird danach in konzentrierte Schwefelsäure eingeleitet, wobei Oleum gebildet wird. Schließlich wird das Oleum mit Wasser verdünnt, um die gewünschte Konzentration von Schwefelsäure (H2SO4) herzustellen. Diese Reaktion verdeutlicht die komplexe Molekülstruktur und die Bedeutung der Polarität sowie der chemischen Bindungen von Wasser in verschiedenen Prozessen.
Durch das Verständnis der Naturwissenschaften und der Kohlenstoffverbindungen, können zahlreiche chemische Reaktionen gezielt genutzt werden, um wertvolle Produkte herzustellen, wie etwa in der anorganischen Chemie. Schwefelsäure spielt vor allem in der industriellen Fertigung und Verarbeitung eine wichtige Rolle und gilt als einer der am häufigsten produzierten chemischen Stoffe weltweit.
Synthese von Polyethylen durch Ziegler-Natta-Polymerisation
Die Synthese von Polyethylen durch die Ziegler-Natta-Polymerisation ist ein bedeutender Schritt in der Herstellung von Kunststoffen. Polyethylen, eine Art Kunststoff, wird weitverbreitet für Verpackungen, Behälter und in vielen anderen Anwendungen genutzt. Die Ziegler-Natta-Katalysatoren ermöglichen diese Polymerisation unter relativ milden Bedingungen.
Ziegler-Natta-Katalysatoren verwenden Übergangsmetallchloride und Aluminiumalkyle, um Ethylen in lange Kettenmoleküle zu verwandeln. Diese Reaktion findet bei niedrigen Temperaturen und Drücken statt, wodurch der Prozess energetisch effizient ist. Der entscheidende Vorteil dieser Methode liegt in der Fähigkeit, kontrollierte Polymermoleküle mit spezifischen Eigenschaften herzustellen.
Polyethylen hat zahlreiche chemische und physikalische Eigenschaften, die es besonders nützlich machen. Es ist leicht formbar, widerstandsfähig gegen Feuchtigkeit und Chemikalien und besitzt eine hohe Beständigkeit gegen mechanische Belastung. Diese Eigenschaften machen es zum Hauptbestandteil vieler Konsumgüter.
Durch die exakte Kontrolle über die Molekülstruktur können unterschiedliche Typen von Polyethylen erzeugt werden, wie z.B. Hochdichtes Polyethylen (HDPE) und Niederdichtes Polyethylen (LDPE). Unterschiedliche Polymere entstehen aufgrund der Variationen in der Katalysatorzusammensetzung und den Reaktionsbedingungen.
Zusammengefasst ermöglicht die Ziegler-Natta-Polymerisation eine präzise Steuerung der chemischen Zusammensetzung des Polyethylens, was wiederum die Vielfalt seiner Anwendungen erhöht.
Was ist die Ziegler-Natta-Polymerisation?
Die Ziegler-Natta-Polymerisation ist ein bedeutendes Verfahren in der Polymerchemie, das zur Herstellung von Hochpolymeren wie Polyethylen und Polypropylen verwendet wird. Dieser Prozess wurde unabhängig voneinander von den deutschen Chemikern Karl Ziegler und Giulio Natta entwickelt, wofür sie 1963 den Nobelpreis für Chemie erhielten.
Bei der Ziegler-Natta-Polymerisation wird ein spezifischer Katalysator, wie beispielsweise ein Titan-Katalysator in Kombination mit einem Cokatalysator wie Alkylaluminiumverbindungen, eingesetzt. Diese Katalysatorsysteme ermöglichen die gezielte Herstellung von Polymeren mit genau definierten Strukturen und Eigenschaften.
Das Verfahren bietet eine präzise Kontrolle über die Polymerisationsreaktion und ermöglicht die Herstellung von Polymeren mit hoher Reinheit und engen Molekulargewichtsverteilungen. Die Ziegler-Natta-Polymerisation wird in der Kunststoffindustrie weit verbreitet eingesetzt, um eine Vielzahl von Kunststoffprodukten mit unterschiedlichen Eigenschaften herzustellen.
Herstellung von Methan durch Fischer-Tropsch-Synthese
Die Herstellung von Methan durch Fischer-Tropsch-Synthese ist ein wichtiger Prozess in der chemischen Industrie. Diese Methode ermöglicht die Umwandlung von Kohlenmonoxid und Wasserstoff in verschiedene Kohlenwasserstoffe, darunter auch Methan.
Im ersten Schritt werden Wasserstoff (H2) und Kohlenmonoxid (CO) für das Verfahren benötigt. Diese Gase entstehen typischerweise durch die Vergasung von Kohle oder die Dampfreformierung von Erdgas. Die Gase werden dann in einem Reaktor unter hohem Druck und hoher Temperatur zusammengeführt.
Ein Katalysator, oft auf Basis von Eisen oder Cobalt, spielt eine zentrale Rolle bei dieser Reaktion. Durch den Einsatz des Katalysators wird die Rate der chemischen Reaktionen erheblich gesteigert, wodurch Methan und andere wertvolle Kohlenwasserstoffe entstehen.
Der eigentliche chemische Prozess verläuft über mehrere Stufen und bildet dabei eine Vielzahl von Nebenprodukten. Methan wird dabei jedoch gezielt kontrolliert hergestellt. Der Endprozess liefert nicht nur Methan (CH4), sondern auch flüssige Treibstoffe wie Diesel und Wachse, was diesen Prozess besonders vielseitig macht.
Diese Synthesemethode hat besondere Bedeutung im Kontext der alternativen Energienutzung und der Verringerung von Abhängigkeiten von traditionellen fossilen Brennstoffen. Innovativ an diesem Prozess ist vor allem seine Flexibilität hinsichtlich der Ausgangsmaterialien, die sowohl biogen als auch fossil sein können.
Durch den Fischer-Tropsch-Prozess kann somit gezielt Methan produziert werden, welches entweder direkt genutzt oder weiter zu anderen chemischen Verbindungen verarbeitet werden kann.
Was ist die Fischer-Tropsch-Synthese?
Die Fischer-Tropsch-Synthese ist ein chemisches Verfahren zur Umwandlung von Synthesegas, einer Mischung aus Kohlenmonoxid und Wasserstoff, in langkettige Kohlenwasserstoffe wie Paraffine und Olefine. Dieser Prozess wurde von den deutschen Chemikern Franz Fischer und Hans Tropsch in den 1920er Jahren entwickelt.
In der Fischer-Tropsch-Synthese reagiert das Synthesegas unter hohen Temperaturen und Drücken in Gegenwart eines Katalysators, typischerweise eines Cobalt- oder Eisenkatalysators. Dabei entstehen verschiedene Kohlenwasserstoffprodukte, die als Kraftstoffe oder chemische Rohstoffe verwendet werden können. Diese Synthese ist besonders wichtig für die Herstellung von synthetischen Kraftstoffen und anderen Kohlenwasserstoffprodukten aus Kohle, Erdgas oder Biomasse.
Die Fischer-Tropsch-Synthese spielt eine wichtige Rolle in der chemischen Industrie als alternative Möglichkeit zur Herstellung von Kohlenwasserstoffen, insbesondere in Regionen, in denen herkömmliche Rohölquellen begrenzt sind.
Synthese von Aspirin durch Acetylierung von Salicylsäure
Die Synthese von Aspirin erfolgt durch die Acetylierung von Salicylsäure, ein Prozess, der als einfache organisch-chemische Reaktion klassifiziert wird. Während dieser Reaktion wird die Hydroxylgruppe der Salicylsäure mit einer Acetylgruppe verknüpft, indem Essigsäureanhydrid zugegeben wird.
Dabei spielt die chemische Zusammensetzung eine entscheidende Rolle. Aspirin, auch als Acetylsalicylsäure bekannt, besteht aus einem H2O Molekül in seiner Struktur und ist deshalb ein Hauptbestandteil vieler flüssiger Medikamente. Seine Eigenschaften resultieren aus der Polarität und den speziellen chemischen Bindungen, die im Molekül vorliegen.
Ein weiterer wichtiger Aspekt bei der Herstellung von Aspirin ist die sorgfältige Kontrolle der Reaktionsbedingungen. Die Temperatur und der pH-Wert müssen optimal eingestellt werden, um die gewünschte Verbindung von Wasserstoff und Sauerstoffgruppen am Kohlenstoffgerüst sicherzustellen. Dies ermöglicht, dass das Molekül seine typische Molekülstruktur beibehält.
Aspirin zeigt beispielhaft, dass selbst in der anorganischen Chemie, wo oft kohlenstofffreie Moleküle erstellt werden, Verbindungen wie Aspirin aufgrund ihrer besonderen Kohlenstoffverbindungen eine wichtige Rolle spielen. Durch diese detaillierte Methode zeigen sich die vielfältigen Anwendungen der Naturwissenschaften und deren Möglichkeiten zur Definition zwischen organischen und anorganischen Stoffen auf.
Ebenso verdeutlicht diese Synthese die Komplexität der chemischen Reaktionen mit Wasser sowie anderen chemischen Elementen und Verbindungen, denen täglich begegnet werden kann.
| Chemische Reaktion | Verfahren | Ergebnisse |
|---|---|---|
| Haber-Bosch-Verfahren | Synthese | Ammoniak |
| Kontaktverfahren | Katalytische Oxidation | Schwefelsäure |
| Fischer-Tropsch-Synthese | Hydrierung | Methan |
| Ziegler-Natta-Polymerisation | Polymerisation | Polyethylen |
| Acetylierung von Salicylsäure | Acetylierung | Aspirin |
| Chloralkali-Elektrolyse | Elektrolyse | Chlor und Natriumhydroxid |
| Fermentation von Glukose | Fermentation | Ethanol |
| Polykondensation | Polymerisation | Nylon |
Produktion von Chlor und Natriumhydroxid durch Chloralkali-Elektrolyse
Um Chlor und Natriumhydroxid gezielt herzustellen, wird die sogenannte Chloralkali-Elektrolyse verwendet. Dieses Verfahren nutzt die elektrolytische Spaltung von gesättigter Natriumchlorid-Lösung (Salzlösung), um Chlor (Cl₂), Wasserstoff (H₂) und Natriumhydroxid (NaOH) zu gewinnen.
Bei dieser chemischen Reaktion spielt die Stromzufuhr eine entscheidende Rolle. Die Anode ist positiv geladen und zieht die negativ geladenen Chloridionen an. Diese geben dort ihre Elektronen ab und bilden Chlor-Gas. An der Kathode, die negativ geladen ist, werden Wasserstoffionen reduziert und es entsteht Wasserstoffgas.
Zwischen den beiden Elektroden wird durch eine Membran oder ein Diaphragma verhindert, dass Chlor und Natriumhydroxid sofort wieder miteinander reagieren. Dies ermöglicht eine effiziente Trennung der einzelnen Produkte.
Die dabei verwendeten Stoffe, wie beispielsweise die gesättigte Natriumchlorid-Lösung, haben eine spezifische chemische Zusammensetzung. Das Produkt, Natriumhydroxid, ist ein unverzichtbares Material in zahlreichen Anwendungen, sowohl in der chemischen Industrie als auch in alltäglichen Produkten.
Diese Methode zeigt eindrucksvoll, wie die Naturwissenschaften genutzt werden können, um komplexe Substanzen aus grundlegenden Verbindungen von Wasserstoff und Sauerstoff zu isolieren. Der gesamte Prozess formt ein beeindruckendes Beispiel für anorganische Chemie im industriellen Maßstab.
Was ist eine Chloralkali-Elektrolyse?
Bei der Chloralkali-Elektrolyse handelt es sich um ein Verfahren, bei dem Natriumchlorid (Kochsalz) in seine Bestandteile Natriumhydroxid (Natronlauge) und Chlor aufgespalten wird. Dieser Prozess findet in einer Elektrolysezelle statt, in der eine elektrische Stromquelle verwendet wird, um die Elektrolyse des Natriumchlorids zu ermöglichen.
Während der Elektrolyse wandern positiv geladene Natriumionen zur Kathode (negativ geladene Elektrode) und werden dort zu elementarem Natrium reduziert. Gleichzeitig wandern negativ geladene Chloridionen zur Anode (positiv geladene Elektrode) und werden dort zu elementarem Chlor oxidiert. Neben Natriumhydroxid und Chlor als Hauptprodukten entsteht auch Wasserstoff als Nebenprodukt an der Kathode.
Die Chloralkali-Elektrolyse ist ein wichtiges Verfahren in der chemischen Industrie zur großtechnischen Herstellung von Natriumhydroxid und Chlor. Es ist ein Beispiel für eine elektrolytische Stoffumwandlung, bei der durch die Anwendung von elektrischem Strom chemische Verbindungen in ihre Bestandteile zerlegt werden.
Herstellung von Ethanol durch Fermentation von Glukose
Die Herstellung von Ethanol durch Fermentation von Glukose ist ein essentieller biochemischer Prozess, der in vielen industriellen Anwendungen genutzt wird. Diese Methode gehört zur anorganischen Chemie und beruht auf der Umwandlung von Zuckerarten wie Glukose zu Ethanol und Kohlendioxid durch die Wirkung von Hefen oder Bakterien.
Der Prozess beginnt mit einer wässrigen Lösung, die reich an Glukose ist, dem Hauptbestandteil von Flüssigkeiten, die für die Gärung geeignet sind. Durch Zugabe von Hefekulturen wird die Glukose in einem aeroben Umfeld fermentiert, wobei die chemische Zusammensetzung des Zuckers entscheidend verändert wird. Die Hefe nutzt Enzyme, um die chemischen Bindungen von Wasser und Glukosemolekülen aufzubrechen und den Zucker in Energie umzuwandeln.
Diese Fermentation führt zur Bildung von Ethanol, einem Kohlenstoff freies Molekül, und Kohlendioxid. Dies ist eine naturwissenschaftliche Anwendung eines einfachen biologischen Prozesses, der aufgrund seiner Effizienz und relativen Einfachheit sowohl in Klein- als auch Großindustrien weit verbreitet ist.
Ethanol selbst hat viele Verwendungen, unter anderem als Kraftstoffzusatz, aber auch in der Kosmetik und Medizin. Seine Polarität macht ihn zu einem nützlichen Lösungsmittel in verschiedenen chemischen Reaktionen. Sein bedeutender Vorteil liegt in seiner umweltfreundlichen Herstellung aus nachwachsenden Rohstoffen wie Pflanzenzucker.
Zusammengefasst stellt die Fermentation von Glukose zur Herstellung von Ethanol eine brillante Kombination aus Biologie und Chemie dar, die sowohl technologisch als auch ökologisch Vorteile bietet.
Synthese von Nylon durch Polykondensation
Die Synthese von Nylon durch Polykondensation ist ein bedeutender industrieller Prozess, der einen speziellen Kunststoff herstellt. Nylon ist eine synthetische Polymerfaser und wird besonders wegen seiner Festigkeit und Elastizität geschätzt.
Dieser Vorgang basiert auf der chemischen Reaktion zwischen Dicarbonsäuren und Diaminen. Ein bekanntes Beispiel ist die Reaktion zwischen Hexamethylendiamin und Adipinsäure. In einer kontrollierten Umgebung verbinden sich diese beiden Moleküle zu einem langen Kettenmolekül, das als Nylon bezeichnet wird.
Im Laufe des Prozesses werden wiederholt Wasserstoff- und Sauerstoffatome abgespalten, wodurch Wasser entsteht. Dies führt zur Bildung zahlreicher Amidbindungen, die für die charakteristische Beständigkeit und Flexibilität von Nylon sorgen. Die Molekülstruktur dieses Materials ermöglicht es, in unterschiedlichen Formen und Anwendungen eingesetzt zu werden, von Textilfasern bis hin zu technischen Kunststoffen.
Insgesamt stellt die Polykondensation eine effektive Methode dar, um Nylon zu erzeugen, welches vielseitig in verschiedenen Industrien genutzt wird. Die chemische Zusammensetzung dieses Materials unterstreicht seine Rolle als Hauptbestandteil robuster und langlebiger Produkte.